Иммунитет после гриппа

Из года в год люди подвергаются заражению гриппа и других инфекций. Если отсутствует иммунитет, переболеть можно 2, а то и 3 раза за сезон. Это связано с тем, что возбудители постоянно мутируют, ежегодно выявляется их новый серотип, в отношении которых бездейственна прошлая вакцина. Поэтому нельзя точно сказать, сколько именно сохраняется иммунитет после гриппа.
Содержание:
-
Парадоксальные суждения об иммунитете при гриппе
-
Сколько сохраняется иммунитет после гриппа
-
Иммунитет после гриппа
-
Иммунитет после вакцинации
-
Факторы длительности иммунитета
-
Вакцинация
Парадоксальные суждения об иммунитете при гриппе
Любое инфекционное заболевание, в том числе грипп, способствует развитию иммунитета. Такой защитный ответ непрочный, поскольку за всю жизнь люди болеют гриппом большое количество раз.
Однако исследования, проводимые над лабораторными животными, несут противоречивый характер. Основываясь на данных эксперимента можно судить о стойко выработанном иммунитете после контактного инфицирования или путем вакцинации. У животных после перенесенного заболевания, формируется долгосрочный иммунный ответ на повторное заражение.
Согласно проведенным опытам, иммунитет животных намного лучше, если инфицирование произошло через носовые ходы. Такой феномен подтверждает наличие местного и общего иммунитета.
Однако далеко не каждый эксперимент можно перенести на людей. Поскольку длительность жизни между организмами сильно различается, что немаловажно при формировании высокой восприимчивости к вирусным заболеваниям.
После выявления мутагенности возбудителя, стало ясно наличие повторного заражения. Болезнь проявляется не из-за слабого иммунитета к вирусу, а в результате изменчивости его генной структуры.
Этот факт подтверждается эпидемией, которая вспыхнула в середине прошлого века. Вначале был один серотип возбудителя, по истечению 20 лет появился новый. И только после повторного развития болезни, вызванной первым вариантом вируса, большее количество зараженных лиц были молодые люди до 20 лет, которые не захватили первую волну. Люди старшего возраста не заражались либо переносили патологию в легкой форме. Это подтверждает тот факт, что иммунитет после гриппа существует, однако он не долгий и имеет узкую направленность.
Сколько сохраняется иммунитет после гриппа
Полная гарантия повторного заражения вирусным заболеванием отсутствует. Поскольку иммунитет не вырабатывается пожизненно. Считается, что максимально защитный ответ на инфекцию может сохраняться до 3-4 лет. Но редко он превышает 1 год, поскольку часто клетки возбудителя подвергаются мутационной изменчивости.
Иммунитет после гриппа
Грипп наиболее опасная и заразная форма вирусных заболеваний, поражающая взрослых и детей.
Распространяется преимущественно воздушным путем. Главным источником патологии выступает больной человек.
Болезнь характеризуется выраженной клинической картиной, часто тяжелым течением с высоким риском развития осложнений. Поэтому начать лечебные мероприятия важно, как можно раньше. Терапию следует проводить до полного устранения вирусных клеток из организма человека.
Поскольку инкубационный период патологии короткий, симптомы появляются внезапно, болезнь быстро прогрессирует. Это влечет к возникновению неблагоприятных последствий. Тяжелые формы патологии характеризуются нарушением функции важных систем, отмечается значительный вред здоровью.
При своевременном обращении к врачу, симптомы удается купировать и влиять на саму причину заболевания. В таком случае наблюдается выздоровление, происходит формирование иммунитета именно к данному типу вируса. При его мутации, имеющийся иммунитет не активен.
Иммунитет после вакцинации
Для защиты населения от различных вирусных инфекций, фармацевтическим служба и лабораториям приходится ежегодно создавать новые формы препаратов. Поскольку вирусные клетки регулярно подвергаются мутагенным процессам.
Такой приобретенный иммунитет будет активен через 3 недели после введения, и продолжит защиту организма в течение года к определенному типу возбудителя. Поэтому вакцинацию рекомендуется проводить в середине или начале ноября, чтобы в сезон гриппа быть готовым к атаке возбудителя.
Однако лекарственное средство не может полностью гарантировать отсутствие заражения. Если произойдет инфицирование, то на фоне вакцинации, клиническая картина будет облегчена, болезнь пройдет быстро и без осложнений.
Факторы длительности иммунитета
Длительность иммунного ответа на воздействие возбудителя гриппа зависит от ряда факторов:
-
Индивидуальная резистентность. Определяется возрастом, образом жизни, анамнезом заболеваний, гормональным и психоэмоциональным фоном.
-
Уровень восприимчивости к гриппу. Всецело зависит от коллективного иммунитета, характера гриппозного заболевания. Замечено, после эпидемии, коллективный иммунный ответ наиболее сильный. Особо длительный иммунитет регистрируется в отношении вирусов В, С. Низкая восприимчивость организма отмечается к вирусу А, что объясняется его частой мутагенностью.
Вакцинация
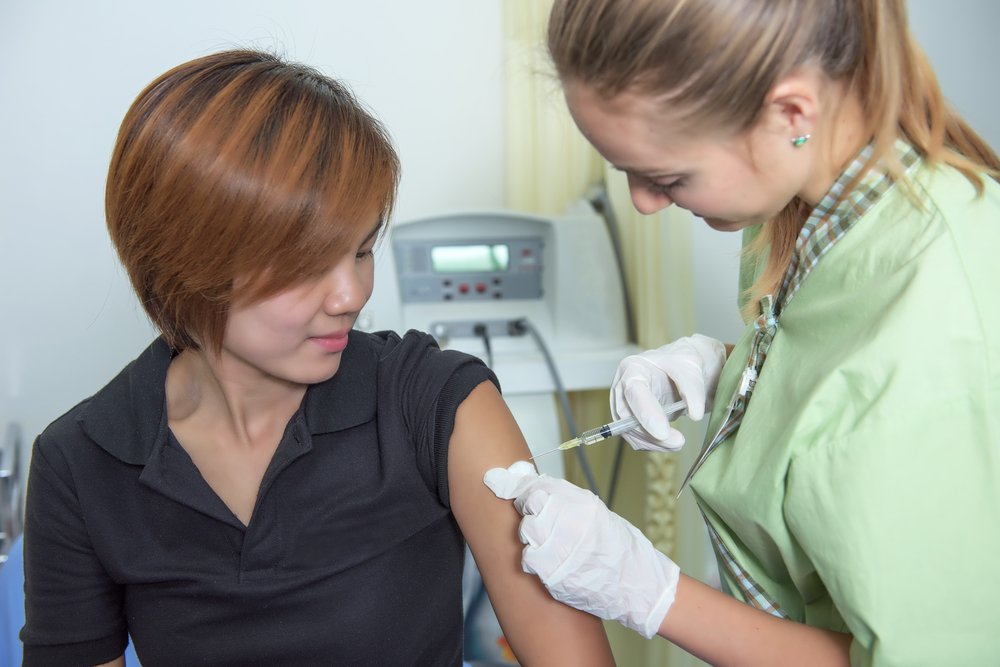
Для облегчения течения болезни или ее предупреждения, людям делают вакцинацию. Она представляет собой неактивные клетки возбудителя, против которых организм синтезирует антитела.
Помимо вакцины, существуют другие методы повышения защитных сил.
Есть особый перечень лиц, которым такой способ крайне показан, это:
-
Беременные женщины.
-
Сотрудники детского сада.
-
Медицинские работники.
-
Пожилые люди.
-
Лица с хроническими болезнями и низким иммунитетом.
Введение препарата с ослабленными вирусными клетками осуществляется место или парентерально.
Грипп — ежегодная напасть, но на этот раз дело осложняется царящим во всем мире вирусом SARS-CoV-2. Насколько важна в такой ситуации прививка от гриппа? Кто определяет, какой штамм будет актуален в этом году? Может ли прививка от гриппа спасти от коронавируса? А от пневмонии?
На все наши каверзные вопросы ответила Елена Михайловна Шабалинская, врач-терапевт 1 квалификационной категории медицинского центра «Эксана».

«Часто люди проявляют нерешительность в вопросе вакцинации»
— Как защитить свое здоровье в осенне-зимний период?
— Когда в воздухе кругом летают вирусы, один из способов защитить себя — заблаговременно привиться от гриппа. Часто люди проявляют нерешительность в этом вопросе, и это неудивительно. Слишком уж много слухов и противоречивых фактов на тему противогриппозных вакцин существует.
Многих останавливает тот факт, что вакцина не может защитить на 100%, а обеспечивает лишь «умеренную защиту» от сезонного гриппа. Однако, когда дело касается здоровья, и такой результат неплох.
Врачи советуют каждому человеку, начиная с 6-месячного возраста, каждый год прививаться от гриппа.
И все же решение по этому вопросу стоит принимать после тщательной оценки для себя всех плюсов и минусов вакцинации от гриппа.

«Вакцина не может сама по себе стать причиной развития инфекции»
— Так стоит ли делать прививку от гриппа? Какие аргументы «за» существуют?
- Прививка способна спасти жизнь. Факт: ежегодно в эпидемически неблагополучный период гриппом заболевают 10% населения, из которых порядка 650 тысяч умирают. Так что это не просто красивые слова, а объективная реальность.
- Прививка сама по себе не вызывает болезнь. Безусловно, в вакцине против гриппа содержатся штаммы вируса, но они либо полностью неактивные, либо крайне ослабленные. А значит, никакого вреда организму нанести не могут.
Иногда рассказывают о таких ситуациях: всей семьей сделали прививки от гриппа и буквально назавтра заболели. Но, во-первых, сама прививка не может стать причиной заболевания, во-вторых, заболевание не может развиться так быстро. Подобные случаи можно объяснить лишь совпадением: вирус уже присутствовал в организме, а вакцинирование просто наложилось по времени на болезнь. Именно поэтому прививаться нужно заранее, до начала эпидемически неблагоприятного сезона.
- Прививка безопасна. Ранее в кругах некоторых родителей считалось, что содержащийся в вакцине консервант тимеросал может стать причиной возникновения аутизма у детей. К счастью, позже эта гипотеза была неоднократно опровергнута. К тому же подавляющее большинство современных вакцин и вовсе не содержат тимеросала, поэтому тема тем более неактуальна.
- Получить вакцину очень легко. Многие фирмы, бизнесы и предприятия организуют централизованную вакцинацию своих сотрудников. Кроме того, Минздрав контролирует факт вакцинации процента людей, которые обязательно должны быть привиты.
- Сделать прививку небольно. Если вы боитесь крови или уколов, всегда можно выбрать вакцину в форме назального спрея. Такие прививки можно использовать лицам в возрасте от 2 до 49 лет.

«Прошлогодняя вакцина в этом году уже не сработает»
— Какие есть аргументы против?
- Для некоторых людей вакцина от гриппа может быть небезопасна. Например, если у вас аллергия на яйца, о прививке, скорее всего, придется забыть. Дело в том, что вакцины культивируются внутри куриных яиц, вследствие этого препарат может вызвать аллергическую реакцию. Также вакцинацию не производят при наличии острых инфекционных или неинфекционных заболеваний и в периоды обострения хронических заболеваний.
- У прививки есть побочные эффекты. После вакцинации иногда возникают боль, покраснение и отечность в месте укола. Также могут повыситься температура, появиться головная боль. Если эти симптомы проявляются, то, как правило, они не выражены в сильной степени и сами проходят в течение двух суток.
- Вакцина действует только один год. Вирусы постоянно мутируют, изменяются и приспособляются. В каждом сезоне доминировать будут разные штаммы. Так что прошлогодняя прививка в этом году уже, к сожалению, не сработает. По этой причине и рекомендуется вакцинироваться, во-первых, ежегодно, во-вторых, до начала эпидемически неблагоприятного сезона (обычно длится с октября по май).
- Прививка от гриппа не дает 100-процентную гарантию от респираторного заболевания. Во-первых, такой гарантии не дает ни один лечебный и профилактический препарат. Во-вторых, вакцина от гриппа защищает от доминирующих вирусных штаммов этого сезона, но не спасает от остальных осенне-зимних вирусов. В-третьих, если говорить о числах, то, по данным ВОЗ, в среднем вакцина предотвращает порядка 60% случаев инфицирования у здоровых взрослых людей в возрасте 18-64 лет. Если человек, сделавший прививку, все же заболеет, то болезнь будет протекать у него в легкой форме и без осложнений.
- Вакцина начинает работать не сразу после инъекции, а по прошествии в среднем двух недель.
Знание всех плюсов и минусов поможет вам сделать осознанный и взвешенный выбор в вопросе вакцинации от гриппа.

— Кому в первую очередь стоит задуматься о прививке от гриппа?
— Таких категорий несколько. Это:
- дети;
- взрослые старше 65 лет;
- люди, страдающие хроническими болезнями сердца и легких, метаболическими заболеваниями, хроническими поражениями печени, неврологическими расстройствами и иммунодефицитами;
- те, кто часто контактирует с большим количеством людей: преподаватели, воспитатели, продавцы, врачи;
- женщины, планирующие беременность.
Также прививку можно делать беременным женщины на втором-третьем триместре беременности. Грипп у беременной может повлечь за собой развитие пороков у плода или возникновение выкидыша.
«Сотни мировых лабораторий наблюдают за вирусами гриппа»
— Есть ли разница между вакцинами? Чем четырехвалентная отличается от трехвалентной?
— С 2013 года Всемирная организация здравоохранения рекомендует првииваться четырехвалентной вакциной. Это значит, что такая прививка сможет защитить вас от четырех штаммов вируса гриппа.
То, какие штаммы вируса войдут в вакцину, определяется исходя из прогноза, какая вирусная ситуация будет в предстоящем сезоне. Существует грипп А и грипп В. Выбор вирусов гриппа А происходит из большого количества вариантов, но, как правило, он достаточно точен. У гриппа В есть всего две линии, и тут как раз и возникают сложности выбора. Если не угадать, то может получиться, что вакцина окажется не такой эффективной, как хотелось бы, и люди будут страдать от вируса гриппа В той линии, которая не вошла в трехкомпонентную прививку.

Четырехвалентная вакцина содержит обе линии вируса гриппа В, и это дает более надежную защиту и высокую эффективность прививки.
Сотни мировых лабораторий наблюдают за вирусами гриппа. Проводя анализ полученной информации, сотрудники ВОЗ каждый год уже весной дают рекомендации по тому, какие виды вирусов гриппа стоит включить в состав вакцины. За последние два десятка лет предложенные варианты оказались верны более чем в 90% случаев.
В нашей стране можно найти вакцины от гриппа, произведенные в России, Нидерландах и Франции.
— Можно ли обойтись без прививки и предпринимать какие-то другие действия: мыть руки, укреплять иммунитет?
— Ни одно из подобных мероприятий, несмотря на свою оправданность, не дает защиту, сравнимую по надежности с прививкой. Со скепсисом медицина относится и к различным иммуномодуляторам. Их эффективность не доказана, и, например, в Европе в аптеках вы ничего подобного не найдете.

Прививка от гриппа и коронавирус
— Способна ли прививка от гриппа как-то повлиять на коронавирус?
— Косвенно — да. Во-первых, вакцина от гриппа позволяет снизить риск осложнений после респираторного заболевания, и это касается не только гриппа, но и COVID-19. Во-вторых, существует опасность подхватить микс-инфекцию — когда человек заболевает и гриппом, и коронавирусом одновременно. Течение болезни у таких пациентов очень тяжелое. И прививка от гриппа позволяет не допустить подобное.
Также в ключе нынешней опасной эпидемиологической ситуации, связанной с вирусом COVID-19, считается оправданной так называемая прививка от пневмонии — тринадцативалентная вакцина, защищающая сразу от 13 штаммов пневмококков. Она не так распространена, как вакцина против гриппа, да и стоимость ее выше, однако она может защитить от осложнений после респираторных инфекций. Иммунитета «хватает» на пять лет, а противопоказания такие же, как и у вакцины от гриппа.
 По теме: Некогда болеть: как избежать гриппа и укрепить иммунитет
По теме: Некогда болеть: как избежать гриппа и укрепить иммунитет
Грипп – это болезнь, от которой ежегодно страдает множество людей. Осенью организму приходится сталкиваться с множеством проблем, связанных с погодой. Утро уже прохладное, днем часто светит солнышко, на улице понижается температура, бывает ветер с дождем. Такие перепады погоды способствуют простуде или гриппу. И если от простуды мы можем уберечься, укрепляя иммунитет и избегая переохлаждения, от гриппа мы можем защититься только с помощью прививки.
Когда грипп особенно опасен
Заболевание появляется сезонно. Повышенная заболеваемость наблюдается в период с поздней осени до начала весны. Вирус гриппа чаще всего передается воздушно-капельным путем при контакте с инфицированным человеком. Хотя его можно подцепить и контактным путем – вирус гриппа может находиться на коже рук, а также на предметах, которыми пользуется больной.
Вакцинация от гриппа – стоит ли делать прививки?
Конечно! Контакт с вирусом возможен абсолютно в любом месте – дома, на работе, в транспорте или магазине. Иногда достаточно просто поздороваться с больным или воспользоваться теми же предметами, что пользовались носители инфекции.
![]()
Избежать заражения активному человеку довольно сложно. Чтобы минимизировать риск заболевания, нужно сделать прививку от гриппа.
По каким еще причинам стоит делать прививки?
Причина 1. Вакцинация повышает иммунитет к вирусам гриппа
Состав вакцины от гриппа меняется ежегодно. Фармацевтические компании, отвечающие за их производство, разрабатывают состав на основе рекомендаций Всемирной организации здравоохранения (ВОЗ). Изменения нацелены на лучшую защиту от болезни, и руководящие принципы основываются на собранных данных и ожидаемой возможности мутации вирусов гриппа в определенное время года.
Вакцинацию можно проводить в любое время, и через 7-10 дней после вакцинации организм становится невосприимчивым к гриппу.
Причина 2. Вакцинация защищает ребенка от гриппа
Роль вакцинации против гриппа особенно важна для детей. Детские сады и школы – отличные места для быстрого распространения вирусов. Заразиться ребенок может не только от друзей, но и от родителей или братьев и сестер, от прохожих во время прогулок и покупок в магазине. Очень важно обеспечить безопасность детей и принять профилактические меры с помощью вакцины от гриппа.
Родители часто не вакцинируют своих детей, думая, что они из-за прививки заболеют гриппом. Но вакцина не может вызвать грипп, потому что в ней нет живого вируса.
Причина 3. Вакцина не может вызвать грипп, потому что в ней нет живого вируса
Вакцина от гриппа может вызывать или не вызывать легкие и кратковременные симптомы, связанные с вакциной (NOP), например, легкую лихорадку, головную боль, чувство разбитости. Также возможны легкие местные симптомы, такие как боль и отек в месте инъекции, которые быстро исчезают.
Риск осложнений всегда во много раз превышает побочные эффекты вакцин. Гриппозная лихорадка, часто очень сильная, – серьезное заболевание, особенно у детей.
![]()
Причина 4. Вакцинация от гриппа экономит деньги
Каждое заболевание обычно связано с необходимостью приобретения лекарств, рекомендованных врачом. Это может быть довольно дорого, особенно при возникновении осложнений. Тяжелые осложнения требуют не только лечения, но и реабилитации. Сделайте прививку от гриппа, чтобы потом не нести лишних расходов.
Причина 5. Благодаря прививке от гриппа вам не придется испытывать мучительные симптомы
Симптомы гриппа включают: боль, слабость, повышенную температуру и др. Тот, кто когда-либо болел гриппом, знает, что такое состояние более, чем неприятно. Избежать этого помогает вакцинация против гриппа. Иммунитет, приобретенный через несколько дней после вакцинации, позволяет радоваться жизни, не опасаясь контакта с инфицированным человеком.
Причина 6. Благодаря вакцинации вам не нужно отказываться от любимых занятий
Многие люди осенью из-за частых инфекций вынуждены отказываться от любимых физических занятий – катания на велосипеде, бега, бассейна или строго ограничить их.
Грипп лишает нас всех видов деятельности, и период выздоровления, то есть полное выздоровление, может быть долгим. Вакцинация против гриппа гарантирует, что, несмотря на сезон гриппа, вам не придется отказываться от занятий спортом или других занятий.
Причина 7. Вакцинация помогает снизить риск осложнений от гриппа. Грипп может даже убить
Сезон гриппа связан с увеличением смертности от осложнений гриппа, особенно сердечно-сосудистых заболеваний. Риск настолько велик, что многие крупные информационные агентства публикуют информацию о количестве случаев гриппа и количество смертельных случаев от него. В случае большого количества случаев в данной популяции это называется эпидемией заболевания.
Здравый смысл, или то, что мы получаем при вакцинации
Решение о вакцинации против гриппа должно основываться на здравом суждении:
- анализ осложнений гриппа;
- исключение из повседневной деятельности;
- длительный период восстановления;
- возможные затраты на лечение;
- снижение оплаты труда за время нахождения на больничном непропорционально высоки по сравнению со стоимостью вакцины.
Кроме того, приняв решение о вакцинации, мы снижаем риск заражения наших близких, которые не всегда могут или еще не успели пройти вакцинацию.
Грипп или не грипп?
К сожалению, иногда люди игнорируют первые симптомы гриппа и приравнивают их к простуде. Почему? Оба состояния вызваны вирусами и имеют схожие симптомы. Однако грипп и простуда – это не одно и то же, они различаются, главным образом способом развития болезни, ее продолжительностью и возможностью серьезных осложнений.
Симптомы гриппа – на что обратить внимание?
Грипп – это заболевание, которое может вызывать множество симптомов как общих, так и очень специфических.
Общие симптомы гриппа включают:
- головные боли и боли в мышцах;
- усталость;
- слабость;
- часто высокая температура и озноб.
![]()
![]()
Грипп также вызывает респираторные симптомы, такие как боль в горле и сухой, утомляющий кашель.
В некоторых случаях пациенты сообщают о желудочно-кишечных расстройствах:
- тошнота;
- рвота;
- легкий понос.
Определенные симптомы гриппа должны побудить нас немедленно обратиться за медицинской помощью.
Серьезные симптомы гриппа:
- Одышка и затрудненное дыхание. Дыхание быстрое и тяжелое, часто громкое или хриплое, может сопровождаться стеснением в груди и ощущением одышки;
- Нарушение сознания, летаргия, общая дезориентация, делирий и даже потеря сознания, судороги или проблема с пробуждением больного человека;
- Мышечная слабость, вызывающая проблемы с ходьбой;
- Недостаток объема мочи или резко сниженный диурез, а также сухость во рту, головокружение, низкое артериальное давление;
- Пятна красного или синего цвета вокруг рта, губ или носа;
- Кровохарканье.
Лечение гриппа
В большинстве случаев гриппа достаточно симптоматического лечения, например, приема лекарств, уменьшающих боль, жар и кашель. Тем не менее вы можете предпринять определенные шаги, которые дополнительно помогут организму быстрее бороться с инфекцией и часто более мягко переносить болезнь.
Лучшее средство от гриппа – это хорошо спать и пить много жидкости.
Три составляющих правильного лечения гриппа:
- Покой. Врачи отмечают, что лучшее, что мы можем сделать во время болезни, – это дать организму большую дозу отдыха. В первую очередь стоит «лечь» и не подвергать себя факторам, которые могут ухудшить состояние.
- Противовирусные средства от гриппа.
- Безрецептурные лекарства. Пациентам, которые жалуются на головную боль и высокую температуру можно применять болеутоляющие и жаропонижающие средства.
- Домашние средства. Есть как минимум десяток домашних средств, которые положительно влияют на состояние во время болезни. Например, можно пить молоко с медом и чесноком, чай с малиновым соком, отвары бузины, липы и малины.
![]()
Некоторые постгриппозные осложнения требуют применения антибиотиков. Это имеет место, например, в случае маленьких детей, у которых вирусная инфекция провоцирует бактериальную инфекцию и поражает, например, ухо или носовые пазухи. Тогда антибиотик становится необходимым, но следует помнить, что он не повлияет на сам вирус гриппа, так как борется только с бактериями.
Профилактика гриппа
Профилактика гриппа в первую очередь включает рекомендации по предотвращению контактов с человеком, инфицированным вирусом гриппа. Однако мы не всегда знаем, что человек, с которым мы говорим, уже болен.
Что же делать, чтобы не заболеть гриппом? Чтобы увеличить вероятность избежать болезни, нужно сделать прививку. Вакцина снижает риск заражения гриппом и, если это все-таки это произойдет, смягчает его течение.
Помимо вакцинации, также очень важны в области профилактики, вопросы, связанные с надлежащей гигиеной, в частности, в отношении мытья и дезинфекции рук.
![]()
Люди, которые кашляют или страдают ринитом, должны прикрывать нос и рот при кашле или чихании, чтобы свести к минимуму риск заражения окружающих. Рекомендации по профилактике также предлагают избегать переполненных комнат и мест.
Не менее важно изолировать больного человека от здоровых, чтобы избежать или минимизировать риск распространения болезни.
Вакцинация от гриппа – кто может пройти вакцинацию?
Вакцинация против гриппа, как и другие прививки, требует медицинской квалификации, то есть подтверждения того, что человек может быть вакцинирован в этот день.
Врач,опрашивая и осматривая пациента, получает информацию о состоянии здоровья, хронических заболеваниях или снижении иммунитета. Вакцинацию следует отложить в случае тяжелой острой инфекции или обострения хронического заболевания.
Противопоказания к введению вакцины против гриппа
- аллергия на яичный белок;
- гиперчувствительность к любому компоненту препарата;
- тяжелые реакции на предыдущую прививку.
Также нельзя вакцинировать младенцев в возрасте до 6 месяцев. Поэтому очень важно, чтобы окружающие, особенно родители и старшие братья и сестры, были вакцинированы от гриппа и не стали источником инфекции для ребенка.
По своей социальной значимости грипп находится на первом месте среди инфекционных болезней человека. Заболеваемость гриппом и острыми респираторными вирусными заболеваниями (ОРВЗ) превышает суммарный показатель по всем остальным инфекциям. В период эпидемии гриппа на долю гриппа и ОРВЗ приходится 10-15% случаев временной нетрудоспособности, а в остальное время года — более 80% от всей инфекционной патологии.
Во время эпидемий болезнь может поражать 10-20% всего населения и до 40-60% пожилых людей. Ежегодно в мире число случаев тяжелой формы заболевания гриппом исчисляется миллионами, а количество летальных исходов достигает 200-500 тыс.
Тяжелые клинические осложнения, развивающиеся при гриппе, такие как пневмония, бронхиты, вторичные бактериальные инфекции верхних дыхательных путей (отиты, синуситы), осложнения со стороны нервной и сердечно-сосудистой систем или обострения хронических заболеваний (сахарный диабет, сердечная недостаточность, хронические обструктивные бронхопневмонии и т. п.) весьма часто встречаются среди пожилых и ослабленных людей и представляют для них серьезную опасность. Количество случаев пневмонии во время эпидемий гриппа возрастает до 70%, а бронхитов до 25%. В настоящее время грипп стоит на втором месте (после пневмококковой инфекции) среди причин смерти от инфекционных заболеваний.

Совершенно очевидна необходимость проведения профилактических мер с целью предупреждения этого опасного заболевания. Сегодня общепризнанным и наиболее действенным средством борьбы с гриппом является вакцинопрофилактика.
Современная концепция вакцинопрофилактики гриппа ориентирована, прежде всего, на иммунизацию лиц высокого риска заражения и последствий инфекции. В соответствии с этой концепцией Министерство здравоохранения РФ рекомендует каждый год вакцинировать всех россиян старше 6 месяцев, если они входят в группу риска по возрасту, состоянию здоровья и характеру профессиональной деятельности.
Правильно организованная иммунопрофилактика гриппа сопровождается снижением заболеваемости другими ОРВИ. Это снижение по данным разных авторов лежит в пределах 25-65%.
Вакцинация против гриппа дает высокий экономический эффект. Один рубль, вложенный в прививки, дает от 3 до 6, а по некоторым данным до 25 рублей экономии за счет сокращения затрат на лечение, оплату больничных листов и т.д.
|
Практически перед каждым человеком, заботящимся о своем здоровье и здоровье своих родных и близких, встает вопрос: «Нужно ли делать прививку от гриппа?» |
Вирусы гриппа относятся к таким возбудителям, которые имеют чрезвычайно высокую способность изменяться. Поэтому наша иммунная система, встретившись с измененным вирусом гриппа, начинает воспринимать его как новый, ранее не известный вирус. И пока иммунная система «налаживает» производство защитных антител, чтобы бороться с вирусом гриппа, у человека развивается заболевание. Именно с изменчивостью вирусов гриппа связаны ежегодные сезонные подъемы заболеваемости. После вакцинации или перенесенного гриппа в организме формируются защитные антитела, однако они сохраняются чуть более полугода, а затем разрушаются. Когда в следующем году приходит новый вариант вируса гриппа, то он вновь «застает врасплох» нашу иммунную систему и мы снова болеем. В настоящее время существуют различные способы подготовить иммунную систему к этой «встрече». Наиболее эффективный способ – прививка.
|
| Вакцины для профилактики гриппа |
Существуют следующие виды вакцин для профилактики гриппа: живые и инактивированные (т.е. убитые). Что значит живая вакцина? Живая вакцина — это вакцина, которая содержит в своем составе живой вакцинный (т.е. специально созданный для вакцины) вирус гриппа. Что значит инактивированная вакцина? Инактивированная (т.е. убитая) вакцина – это вакцина, которая в своем составе содержат целый убитый вакцинный вирус гриппа либо его отдельные частички (антигены). |
|
Что общего между всеми вакцинами для профилактики гриппа? |
Всевакцины для профилактики гриппа создают надежный иммунитет против заболевания гриппом. |
|
Чем отличаются вакцины для профилактики гриппа? |
Методом введения. Живые вакцины вводятся путем распыления спомощью дозатора. Убитые вакцины вводятся с помощью укола |
| Возраст, с которого можно проводить прививки |
Ультрикс можно вводить детям с6лет. Совигрипп детский можно вводить детям с 6 месяцев и взрослым. Совигрипп взрослый 18лет и старше. Ультрикс–является инактивированной вакциной,то есть вирусные телаубиты специальным раствором, и расщеплённой — вирусы в ней разбиты на отдельные белки. Убитые вакцины имеют неоспоримое преимущество по сравнению с живыми — они вызывают меньше побочных реакций, а расщепление даёт возможность организму лучше распознать каждый антиген и выработать соответствующую защиту. Применяется для школьников. Каждый год в состав вакцин включаются те варианты вирусов гриппа, которые рекомендуют специалисты ВОЗ. |
|
Когда после прививки против гриппа сформируется защита от заболевания? |
Через 14-21 день после вакцинации развивается иммунитет, который обеспечивает защиту от заболевания гриппом в течение 6-12 месяцев. Гарантирует ли прививка от гриппа 100% защиту от заболевания? 100% гарантию от заболевания не дает ни один лечебный, ни один профилактический препарат. Насколько надежная защита выработается после вакцинации зависит от многих факторов, в т.ч. возраста и состояния здоровья пациента, индивидуальных особенностей и т.д. Но в среднем из 100 привитых 70-98 человек не заболеют гриппом. Если все же привитой человек заболеет гриппом (2-30 человек из 100 привитых), то заболевание у него будет протекать в легкой форме и без осложнений. Таким образом, вакцинация гарантирует защиту от заболевания тяжелыми и осложненными формами гриппа, заканчивающимися смертельным исходом. Вакцина против гриппа предназначена в первую очередь, для защиты именно от вирусов гриппа, а не от других респираторных вирусов. В тоже время вакцина против гриппа обладает дополнительными, в некоторой степени иммуномодулирующими свойствами. Благодаря этому, иммунная система примерно 20-25 человек из 100 привитых приобретает дополнительную защиту и от других респираторных вирусных инфекций.
|
|
Может ли вакцина против гриппа вызвать реакции? |
Введение любых вакцин, в т.ч. вакцин для профилактики гриппа может вызывать реакции. Возникновение температуры или покраснения в месте введения вакцины – это закономерная реакция на любую вакцину, свидетельствующая о начале формирования защиты. После вакцинации против гриппа у привитых могут отмечаться: Общие реакции – это реакции, которые в целом затрагивают организм и проявляются в виде повышения температуры тела, недомогания, головной боли и др. Местные реакции — это реакции, которые проявляются в месте введения вакцины в виде уплотнения и болезненности. Эти проявления кратковременны, не требуют лечения и исчезают самостоятельно в течение 2-3 дней, не нарушая трудоспособности и не требуя дополнительного лечения. |
|
На какие вакцины против гриппа чаще развиваются реакции? |
Чащевозникают общие реакции на введение живых вакцин: из 100 привитых против гриппа у 8-15 человек могут быть общие реакции в виде повышения температуры тела (до 38°С), общего недомогания. Все эти симптомы кратковременны и исчезают самостоятельно. |
|
Противопоказания для вакцинации. Когда нельзя проводить прививки против гриппа? |
Существуют определенные состояния здоровья, когда прививка для профилактики гриппа может быть временно отложена (временные противопоказания) либо прививку вообще нельзя проводить никогда (постоянные противопоказания). В любом случае, решение о противопоказаниях принимает врач, после осмотра и опроса пациента. К временным противопоказаниям к вакцинации против гриппа относятся состояние острого заболевания или обострения хронического заболевания. После нормализации состояния (снижения температуры и выздоровления) или перехода хронического заболевания в стадию ремиссии можно вводить вакцину. Постоянное противопоказание к вакцинации против гриппа устанавливается крайне редко, в случае наличия немедленной аллергической реакции в виде анафилактического шока, крапивницы, отека Квинке на белок куриных яиц (т.к. выращивание вакцинного вируса происходит именно на куриных эмбрионах). Такие реакции имеются у лиц, у которых при попытке съесть куриное яйцо в любом виде (варенное яйцо, яичница и т.д.) у человека немедленно развивается отек нижней губы, горла и т.д. Если таких реакций нет, то вакцинация против гриппа для такого человека безопасна. |
|
Можно ли делать прививку против гриппа, если есть хроническое заболевание сердца? |
Можно и нужно. Хронические заболевания (в т.ч. заболевания сердца) являются не противопоказанием, а показанием к проведению прививки против гриппа. Пациенты с хроническими заболеваниями хорошо переносят вакцинацию и у них развивается достаточная защита от заболевания. Проведенная прививка не приводит к обострению хронического заболевания, в то время как перенесенный грипп с большой долей вероятности может привести к обострению хронического заболевания и утяжелению его дальнейшего течения. Однако, в период обострения хронического заболевания, врач предложит отложить прививку до стабилизации состояния. |
|
Контингенты риска. Для кого грипп наиболее опасен? |
Грипп опасен для каждого, потому что во время сезонного подъема заболеваемости гриппом погибают и здоровые люди. Однако, наибольшую угрозу грипп и его осложнения представляют для маленьких детей, пожилых лиц, а также для людей, страдающих хроническими болезнями. Это, в первую очередь, дети с поражениями центральной нервной системы, пациенты с патологией сердца (врожденные пороки сердца, инфаркт в анамнезе, ИБС и т.д.), с заболеваниями легких, почек, эндокринной системы, с иммунодефицитами и т.д. К сожалению, иногда именно эти состояния ошибочно рассматриваются как противопоказания для проведения вакцинации против гриппа. Хотя такие лица требуют первоочередной защиты. Грипп опасен и для женщин, планирующих беременность. Целесообразно вакцинироваться до беременности или во время второго-третьего триместра. Заболевание гриппом беременной женщины может повлечь развитие пороков у плода или возникновение выкидыша. Грипп актуален и для лиц, которые в силу особенностей профессии (преподаватели, воспитатели, продавцы, врачи, другие лица, работающие в коллективах) контактируют с большим количеством людей и имеют высокий риск заражения гриппом. |
|
О ежегодной вакцинации против гриппа и выборе вакцин Необходимо ли прививаться в нынешнем году, если делал прививку в прошлом? |
Защитные антитела, выработанные после прививки, обычно в течение 6-12 месяцев после вакцинации разрушаются или их количество становится недостаточным для защиты от гриппа в новом сезоне. Кроме того, ежегодно обновляются варианты вирусов гриппа, которые входят в состав вакцин. Так что стоит прививаться ежегодно. |
|
Как лучше прививаться:одной и той же вакциной каждый год или их лучше менять? |
Учитывая, что ежегодно варианты вирусов гриппа в составе всех вакцин одинаковы, целесообразность смены понравившейся Вам вакцины отсутствует. их использования у грудных детей, начиная с 6 месяцев, людей с хроническими заболеваниями, у беременных и кормящих грудью женщин. |
|
Можно ли заболеть гриппом после прививки и заразить окружающих? |
При вакцинации любой вакциной заболеть гриппом нельзя. Так как в процессе производства вакцинные вирусы лишаются свойства вызывать заболевание, однако сохраняют способность формировать защиту. При вакцинации живой вакциной риск заражения вакцинным вирусом окружающих крайне низкий. В случае вакцинации инактивированными вакцинами против гриппа риск заражения окружающих вакцинным вирусом отсутствует. |
|
Нужно ли как-нибудь готовиться к вакцинации против гриппа? |
Большинству людей специальной подготовки к вакцинации против гриппа не требуется. Отдельным пациентам (например, с аллергическими заболеваниями) врач может назначить медикаментозную подготовку. У больных хроническими заболеваниями вакцинация проводится на фоне приема обычной терапии. |
|
Можно ли прививать ребенка, если он больше 4-х раз в год болеет простудой? |
Не только можно, но и нужно. Именно такой ребенок наиболее подвержен осложнениям, развивающимся после перенесенного гриппа. Прививать такого ребенка необходимо в период отсутствия у него острого заболевания.
|
|
Можно ли прививаться, если я перенесла простуду, а кашель остался? |
Не рекомендуется прививаться в период острого заболевания. Что же касается остаточных явлений, но они не являются противопоказанием, но в любом случае ваше состояние перед прививкой оценит врач, который и примет окончательное решение. |
|
Если я не успел привиться до эпидемии гриппа, то можно ли привиться во время эпидемии? |
Широко распространено мнение, что после начала подъема заболеваемости гриппом вакцинация противопоказана. Это имеет отношение к живым противогриппозным вакцинам. Инактивированные вакцины можно применять на протяжении всего сезона подъема заболеваемости гриппом, если риск заболевания достаточно высок. Однако, если прививка была сделана тогда, когда человек уже заразился вирусом гриппа (но симптомы еще не проявились), то вакцинация окажется неэффективной. |
|
Почему взрослым вводят одну дозу вакцины, против гриппа, а некоторым детям советуют две? |
Это связано с наличием у взрослых иммунологической памяти в отношении вирусов гриппа, поэтому одной дозы достаточно для того, чтобы ее «освежить». Маленьким детям вводят 2 дозы только в первый год вакцинации. В последующие годы для формирования эффективной защиты им достаточно одной прививки. |
|
Можно ли за один раз привиться от гриппа и дифтерии? |
Вакцину против гриппа можно совмещать с любой другой вакциной, кроме вакцины против туберкулеза. Единственным условием является то, что обе вакцины будут введены в разные участки тела. |
|
В прошлом году сделал прививку от гриппа, но все равно заболел. Смысл этой прививки? |
Существует 2 варианта объяснения этой ситуации. Во-первых, наряду с вирусом гриппа заболевание у человека может вызывать более 200 видов других респираторных вирусов. Причем, отличить эти заболевания по клиническим симптомам практически невозможно. Поэтому, если Вы сделали прививку и у Вас возникло заболевание с повышением температуры, головной болью, слабостью, то это не значит, что развился грипп. Вероятнее, всего, что это другая вирусная инфекция, потому что от гриппа Вы защищены. И нам важно защитить Вас именно от гриппа – от той инфекции, которая дает наибольшее количество осложнений и смертельных исходов. Во-вторых, есть небольшая вероятность, что у Вас развился грипп. Насколько тяжело он протекал? С большой уверенностью отвечу – у вас не было тяжелых осложнений. А если бы Вы не сделали прививку и заразились гриппом, то такие осложнения могли бы быть и исход заболевания мог бы быть неблагоприятным. Редко, но встречаются ситуации, когда человек сделал прививку и «встретился» с вирусом гриппа» в тот период, когда защита еще не успела сформироваться. А для выработки достаточной защиты необходимо 14-21 день. Поэтому, прививку от гриппа, делать все-таки стоит. |
|
Есть мнение (в частности, приверженцев нетрадиционной медицины), что вакцинация вредна детям. Они утверждают, что в период, когда у ребенка еще только формируется иммунитет, организм только начинает сам его вырабатывать, введенная вакцина якобы его угнетает и ослабляет организм. И вообще любая прививка снижает возможность у детского организма самостоятельно вырабатывать иммунитет. Может она и не нужна малышам? |
Это совершенно не так. Наоборот, вакцина – это самая слабая тренировка иммунной системы. Система учится работать с антигеном. Но если эти антигены безопасны в плане осложнений, то при встрече с дикими возбудителями, иммунная система будет работать гораздо интенсивнее и ее тренировка будет идти через болезнь. А болезнь – это всегда риск осложнений, и даже смертельного исхода. Я совершенно не соглашусь с утверждениями, что прививкой мы расслабляем иммунную систему, что она будет работать только с вакцинами и хуже реагировать на какие-то другие возбудители. Для такого утверждения нет ни теоретических, ни практических оснований. Но, что касается маленьких деток, то они действительно очень уязвимы. Если у малыша нет братиков и сестричек, который могут «принести» грипп из школы либо детского садика, родители живут не в общежитии, а в собственной квартире, то, может быть, и не стоит защищать его при помощи вакцины. Вероятность заражения в такой ситуации минимальная. Но если есть старший ребенок, посещающий школу, то риск подхватить вирус есть, и в таком случае вакцинация оправдана. Ведь показатели заболеваемости среди детей обычно в два-три раза выше, чем у взрослых. А 90 процентов госпитализированных при гриппе – дети. У них заболевание протекает тяжело и именно их надо защищать в первую очередь. |
|
Когда лучше делать прививку от гриппа? |
Лучше всего прививаться от гриппа осенью: в сентябре-ноябре, до начала сезонного подъема заболеваемости гриппом и ОРИ. В течение 2-3 недель после вакцинации сформируется защитный уровень антител против вирусов гриппа. |
|
Где можно привиться от гриппа? |
Привиться можно в поликлинике по месту жительства, в участковых больницах и амбулаториях, на ФАПах. Отдельным контингентам риска вакцинация проводится на бесплатной основе. В настоящее время все больше и больше руководителей предприятий, заботясь о здоровье своих сотрудников, закупают вакцину от гриппа для их иммунизации. Для удобства вакцинации работающих на предприятиях организуются выездные прививочные бригады. В составе выездной бригады в обязательном порядке присутствует врач, который осуществит осмотр пациентов и определит показания и противопоказания к вакцинации. Остальному населению предоставляется возможность вакцинироваться на платной основе. |
|
Почему в коллективе рекомендуют прививать 40% работающих? |
Действительно, рекомендуется охватывать вакцинацией против гриппа не менее 40% работающих в коллективе. При этом достигаются две основные цели. Первая цель — индивидуальная защита привитого человека. Вторая цель – формирование коллективного иммунитета среди работающих. Коллективный иммунитет дает дополнительную степень защиты привитым и снижает вероятность заболевания непривитых членов коллектива. Чем больше привитых, а значит защищенных от гриппа, тем ниже вероятность заноса и распространения вируса среди работающих в коллективе. При охвате менее чем 40% работающих, коллективный иммунитет практически не работает. Безусловно, максимального эффекта от вакцинации против гриппа, как и при других инфекциях, можно достичь, если в коллективе привиты более 95% работающих. Однако, при вакцинации против гриппа достичь таких показателей сложно, учитывая, что вакцинация проводится в предэпидемический сезон в течение 2-3-х месяцев. Таким образом, охват вакцинацией против гриппа не менее 40% работающих в коллективе обеспечивает индивидуальную защиту привитого и формирует дополнительные возможности защиты за счет коллективного иммунитета. |
| Как будут прививать против гриппа детей в школах и детских садах? |
Родителей в письменной форме информируют (а возможно и устно, на родительском собрании) против чего и каким образом будут прививать их детей, какую вакцину будут использовать. Затем родители подписывают согласие (либо отказ) по установленной форме. Оно хранится в медицинской документации ребенка. В определенный день в школу (садик) приезжает прививочная бригада (врач и медсестра) и проводят вакцинацию. Если мама захочет присутствовать при проведении ребенку прививки, она вместе с ним может обратиться в поликлинику по месту жительства. |
На сегодняшний день существует множество инфекций, борьба с которыми протекает с переменным успехом. Находят новые методы их уничтожения, и тут же вирусы приобретают иные свойства и перестраиваются. Помогает в этой борьбе вакцина, и на каждый вид инфекции предполагается свой вариант. Открытые этого метода определило новый путь развития науки в борьбе с болезнями.
Что представляет собой вакцина?
С первых дней жизни малышей прививают. В состав вакцины входят микроорганизмы или их части. Их искусственно ослабляют, и они выступают в роли муляжа, с помощью которого иммунная система учится правильно реагировать на атаки вирусов.
Итак, вакцина представляет собой препарат, в составе которого находится минимальное количество ослабленных возбудителей инфекции. Заболеть в полной мере после прививки невозможно, но этот метод позволяет организму зафиксировать характерные признаки микроорганизмов. Если он столкнется в будущем с подобной инфекцией, то, определив угрозу, ее устранит.
Уже в течение века в широком смысле используют вакцинацию для обезвреживания бактерий и вирусов. Аттенуация — ослабление возбудителей инфекции.
Предупреждение инфекции: методы борьбы
Все препараты для иммунизации делят на классы, и их насчитывают три:
- живые вакцины;
- инактивированные;
- анатоксины.
Живые вакцины применяют против инфекций таких, как:
- полиомиелит;
- корь;
- ветрянка;
- туберкулез;
- краснуха;
- грипп;
- ротавирусная инфекция.
Специальным способом ослабленные возбудители болезни входят в состав препарата.
Такие серьезные и опасные заболевания, как тиф, в том числе и брюшной, бешенство, гепатит А и другие, нейтрализуют с помощью вакцин инактивированных, в состав которых включены нежизнеспособные микроорганизмы либо их фрагменты.
В третьем варианте с применением анатоксинов обрабатывают токсины бактерий, и делают это по специальной технологии. Так получают вакцину против столбняка, коклюша и др.
Новым веяньем в этой сфере стали молекулярные вакцины, содержащие в своем составе вещества, полученные с применением методов генной инженерии. Виросомальные вакцины способны усилить иммунный статус и имеют побочный эффект встречается реже.
Температура и слабость после прививки
Грипп знаком каждому из нас, и нет, пожалуй, человека, хоть однажды не испытавшего на себе действия вирусной инфекции. Предотвратить эпидемию помогают прививки и, как утверждают специалисты, шанс заболеть существенно снижается.
Распространяется инфекция молниеносно, поражая практически всех, кто попадает в радиус воздействия вируса. Но все по-разному реагируют на нее, так как иммунный статус отличается.
Вирус внедряется в слизистую оболочку, а зачастую это органы где предполагается распространение инфекции воздушно-капельным путем. Клетки разрушаются, а отторгнутые заражают окружающих при кашле и чихании.
Плюсы и минусы вакцинации
Существует много мнений за и против данного мероприятия. У некоторых сразу после прививки поднимается температура, человек начинает чувствовать недомогание. Но в любом случае заболевание протекает в более легкой форме.
Правда, есть и большая ложка дегтя в этом бочонке со сладкими увещеваниями о защите от вирусов. Коварство состоит в том, что он мутирует и меняется год от года, а в новом сезоне есть вероятность столкнуться с той его разновидностью, которая плохо реагирует на все профилактические меры.
Организм способен самостоятельно выработать иммунитет против вируса гриппа, но он постоянно изменяется, и появляются все более устойчивые к лекарственным препаратам типы.
Существует инактивированные и живые типы вакцин, но вторые уже практически не применяют по той причине, что вирус гриппа постоянно совершенствуется. Проводится анализ вируса, и подбирается состав вакцины.
Невозможно предсказать точно, что в этом году будет активным определенный тип вируса, поэтому дать 100% гарантию того, что привитый человек не заболеет, нельзя. Но в любом случае риск заражения у привитых людей гораздо ниже чем у тех, кто не проходит вакцинацию.
Несмотря ни на что прививка — лучший вариант для защиты от инфекций, особенно в период эпидемий. Когда в 90-е годы многие отказывались от вакцинации резко поползла вверх кривая многих заболеваний. В любом случае прививка в разы безопаснее реальной болезни.
Существуют и серьезные аргументы против:
- аллергическая реакция на вакцину;
- некачественный материал;
- возможный риск при воздействии на иммунную систему, особенно ребёнка;
- эффективность не 100%.
По мнению некоторых врачей, приобретенный иммунодефицит возникает у детей из-за неграмотно составленной схемы прививок и плохо контролируемого применения лекарственных средств из группы антибиотиков.
После прививки появляются не только температура, слабость и головная боль, могут наблюдаться и другие симптомы. Место укола иногда воспаляется и возникает нагноение.
Легкое недомогание вполне объяснимо и допустимо, так как организм борется с инфекцией. Температура должна войти в норму в течение трех дней без какого-либо лечения.
Можно ли отказаться от прививок? На основании закона — да, и отказ приема в детский сад или школу без них безоснователен. Только в случае эпидемии могут временно отложить прием документов.
Осложнения
Возможны и побочные эффекты. Среди них: резкое снижение показаний артериального давления, сбои в работе сердечной мышцы, судороги, анафилактический шок. Важно соблюдать все меры предосторожности, а в случае, если здоровье подорвано после вакцинации, выплачивается компенсация.
Противопоказания
Хотя нет иной защиты от болезней, существует часть населения, для которых вакцинация может нанести вред серьезней, чем возможная болезнь. Особенно это касается детей, если это:
- новорожденные с малым весом или недоношенные;
- при их внутриутробном инфицировании;
- наличие гемолитической болезни;
- иммунодефицитные состояния;
- наличие гнойных поражениий кожного покрова;
- наличие заболеваний в острой форме.
Для взрослых людей также есть противопоказания, но с каждым годом этот список уменьшается. Связано такое положение дел с тем, что, как показала практика, при инфицировании корью, краснухой, туберкулезом, заболевания у взрослых протекают в очень тяжелой форме.
Противопоказания подразделяются на:
- Истинные. Описанные в инструкции к вакцине и прилагаемых документах;
- Ложные. Как таковые, пациенты не нуждаются в отводе, так как состояние определяется врачами или самими людьми по личным ощущениям и исходя из ложного чувства жалости;
- Абсолютные. В этом случае никакие другие варианты, кроме отказа от прививки не рассматриваются;
- Относительные. В случаях, когда врач на основании факторов может решать, как лучше поступить: прививать или это нанесет больший вред;
- Временные. При определенных условиях делать прививку не рекомендуют, но при прошествии определенного периода вакцинация вполне допустима;
- Постоянные. Ряд заболеваний, при которых не будет возможности снять запрет;
- Общие. Они касаются всех прививок и отвергаются при остром течении болезни, и если обострилось и хроническое заболевание;
- Частные. В определенный период некоторые прививки нельзя делать, например, беременным. В этом случае требуется внимательно подходить к вакцинации.
Так как современные методы совершенствуются, появляются новые вакцины, в которых соблюдается концентрация балластных веществ. Это позволяет постепенно сокращать список причин, на основании которых рекомендуют отказ от прививок.
Инфекционные болезни. Национальное руководство. / Под ред. Н.Д. Ющука, Ю.Я. Венгерова – 2015
Инфекционные болезни и эпидемиология / Покровский В.И., Пак С.Г., Брико Н.И., Данилкин Б.К. – 2007
- Авторы
- Файлы
Сологуб Т.В.
Ледванов М.Ю.
Малый В.П.
Стукова Н.Ю.
Романцов М.Г.
Бизенкова М.Н.
Полякова Т.Д.
Взаимоотношения иммунитета и инфекции определяют развитие очень многих заболеваний. В полной мере сила и «разумность» инфекции проявляются в примере динамического противостояния живых систем — вирусной инфекции и иммунитета. Если вирус «спрятался» в клетках организма человека и заблокировал их апоптоз, то найти такую инфекцию и избавить организм от нее иммунная система может с помощью Т-клеток -киллеров. Они обнаруживают небольшие фрагменты вирусных белков, встроенных на поверхность инфицированной клетки. Задача Т-киллеров — выявить все инфицированные клетки и убить их путем апоптоза, чтобы не навредить соседним неинфицированным клеткам. Так и происходит в большинстве случаев, но когда Т-клетки-киллеры не обнаруживают признаков инфекции на поверхности инфицированных клеток и превращаются в бесполезное оружие иммунитета, на помощь приходят NK-клетки, имеющие точно такой же аппарат убийства других клеток, как и Т-киллеры. Такой иммунный контроль вирусной инфекции высокоэффективен.
Экспрессия генов ДНК-содержащих вирусов происходит в соответствии с центральной догмой молекулярной биологии: «ДНК — мРНК — белок». В процессе транскрипции участвуют вирусные и клеточные ферменты, как правило, неструктурные белки. По локализации ДНК-вирусы разделяются на ядерные (герпесвирусы, аденовирусы, паповавирусы) и цитоплазматические (вирус оспы). У некоторых из ядерных ДНК-вирусов (паповавирусы, герпесвирусы) возможна интеграция генома в клеточные хромосомы. У крупных ДНК-вирусов сначала синтезируется полицистронная РНК, которая затем нарезается и процессируется. У цитоплазматических ДНК-вирусов транскрипция осуществляется вирусными РНК-полимеразами.
У РНК-содержащих ретровирусов сначала происходит обратная транскрипция генома в ДНК, затем ее интеграция в клеточные хромосомы и лишь после этого транскрипция генов.
Цитопатические эффекты при вирусных инфекциях разнообразны, они определяются как вирусом, так и клеткой и сводятся к разрушению клетки (цитолитический эффект), сосуществованию вируса и клетки без гибели последней (латентная и персистирующая инфекция) и трансформации клетки.
Вовлеченность организма в инфекционный процесс зависит от ряда обстоятельств — количества погибших клеток, токсичности вирусов и продуктов распада клеток, от реакций организма, начиная от рефлекторных и заканчивая иммунными. Количество погибших клеток влияет на тяжесть инфекционного процесса. Например, будут ли поражены при гриппе только клетки носа и трахеи или вирус поразит клетки эпителия альвеол, зависит тяжесть и исход болезни.
Хотя вирусы и не образуют типичных токсинов, однако и вирионы, и вирусные компоненты, накапливающиеся в пораженных тканях, выходя в кровоток, оказывают токсическое действие. Неменьшее токсическое действие оказывают и продукты распада клеток. В этом случае действие вирусной инфекции столь же неспецифично, как и действие патогенных организмов, убивающих клетки и вызывающих их аутолиз. Поступление токсинов в кровь вызывает ответную реакцию — лихорадку, воспаление, иммунный ответ. Лихорадка является преимущественно рефлекторным ответом на поступление в кровь и воздействие на ЦНС токсичных веществ.
Если лихорадка — общий ответ организма на вирусную инфекцию, то воспаление — это местная многокомпонентная реакция. При воспалении происходят инфильтрация пораженных тканей макрофагами, утилизация продуктов распада, репарация и регенерация. Одновременно развиваются реакции клеточного и гуморального иммунитета. На ранних стадиях инфекции действуют неспецифические киллеры и антитела класса IgM. Затем вступают в действие основные факторы гуморального и клеточного иммунитета. Однако гораздо раньше, уже в первые часы после заражения, начинает действовать система интерферона, представляющая семейство секреторных белков, вырабатываемых клетками организма в ответ на вирусы и другие стимулы. Описанные явления относятся к так называемой острой репродуктивной вирусной инфекции. Взаимодействие вируса и клеток может происходить, как отмечалось выше, без гибели последних. В этом случае говорят о латентной, т.е. бессимптомной или персистирующей хронической вирусной инфекции. Дальнейшая экспрессия вируса, образование вирусспецифических белков и вирионов вызывает синтез антител, на этой стадии латентная инфекция переходит в персистирующую и появляются первые признаки болезни.
Репродукция вируса в клетках сопровождается развитием цитопатических процессов, специфичных для разных вирусов и для разных типов инфекционных процессов. Цитопатические процессы при вирусных инфекциях разнообразны, они определяются как вирусом, так и клетками, причем специфика их больше «задается» клеткой, нежели вирусом, и сводится в основном к разрушению клеток, сосуществованию вируса и клеток без гибели последних и трансформация клеток. Несмотря на значительные различия цитоцидного действия разных вирусов, в общем, они сходны. Подавление синтеза клеточных макромолекул — нуклеиновых кислот и белков, а также истощение энергетических ресурсов клетки ведут к необратимым процессам, заканчивающимся гибелью пораженной клетки. Повреждение клеток вирусами, их отмирание и распад переносят вирусную инфекцию с клеточного уровня на уровень организма в целом.
При встрече организма с вирусной инфекцией продукция интерферона (растворимого фактора, вырабатываемого вирус-инфицированными клетками, способного индуцировать антивирусный статус в неинфицированных клетках) становится наиболее быстрой реакцией на заражение, формируя защитный барьер на пути вирусов намного раньше специфических защитных реакций иммунитета, стимулируя клеточную резистентность, — делая клетки непригодными для размножения вирусов.
Продукция и секреция цитокинов относятся к самым ранним событиям, сопутствующим взаимодействию микроорганизмов с макрофагами. Этот ранний неспецифический ответ на инфекцию важен по нескольким причинам: он развивается очень быстро, поскольку не связан с необходимостью накопления клона клеток, отвечающих на конкретный антиген; ранний цитокиновый ответ влияет на последующий специфический иммунный ответ.
Интерферон активирует макрофаги, которые затем синтезируют интерферон-гамма, ИЛ-1, 2, 4, 6, ФНО, в результате макрофаги приобретают способность лизировать вирус-инфицированные клетки.
Интерферон-гамма является специализированным индуктором активации макрофагов, который способен индуцировать экспрессию более 100 разных генов в геноме макрофага.
Продуцентами этой молекулы являются активированные Т-лимфоциты (Тh1-тип) и естественные киллеры (NK-клетки). Интерферон-гамма индуцирует и стимулирует продукцию провоспалительных цитокинов (ФНО, ИЛ-1, 6), экспрессию на мембранах макрофагов, антигенов МНС II; гамма-интерферон резко усиливает антимикробную и противовоспалительную активность путем повышения продукции клетками супероксидных радикалов, а усиление иммунного фагоцитоза и антителоопосредованной цитотоксичности макрофагов под влиянием гамма-интерферона связано с усилением экспрессии Fc-рецепторов для JgG. Активирующее действие интерферона-гамма на макрофаги опосредовано индукцией секреции этими клетками ФНО -альфа. Этот пик наблюдается совместно с ФНО-альфа. Максимум продукции ИЛ-4 наступает через 24-48 ч с момента активации клеток. При этом ИЛ-4 рассматривается как цитокин, ограничивающий иммуновоспалительные реакции и снижающий ответ организма на инфекцию, угнетая при этом экспрессию гамма-интерферона. Интерферон-гамма ин витро усиливает фагоцитарную активность нейтрофилов, что обусловлено усилением экспрессии Fc-рецепторов и поверхностных белков семейства интегринов на нейтрофилы. Это позволяет нейтрофилам осуществлять цитотоксические функции и фагоцитоз. В качестве основных эффекторных клеток воспалительного процесса, они обеспечивают элиминацию инфекта из организма.
Взаимодействие цитокина с клеткой определяется универсальной биологической системой, специфическим механизмом которой является рецепторный аппарат, связанный с восприятием метаболического кода. Для проявления биологической активности цитокина необходимо присутствие на поверхности чувствительных клеток специфических рецепторов, которые могут экспрессироваться параллельно с синтезом цитокина. Рецепторы цитокинов представляют собой комплексы, состоящие из двух и более рецепторных молекул, которые объединяются на мембране клетки-мишени и образуют высокоаффинный рецепторный комплекс. Большинство рецепторов состоит из отдельных молекул, связывающих цитокины, которые ассоциируются после связывания лиганда с сигналпередающим рецепторным компонентом; часть рецепторов существует как растворимые изоформы, способные связывать и растворять цитокины, а часть функционирует как многокомпонентные блоки; механизм комплексирования субъединиц рецепторов объясняет плейотропные и дублирующие эффекты цитокинов, имеющих большое структурное сходство. Рецепторы ИЛ-10 имеют гомологию рецепторов интерферона, и подобно ИЛ-10 индуцирует экспрессию в моноцитах гена Fc- рецептора. Для полного функционирования цитокиновой системы необходимы повышение уровня цитокина в ответ на инфект и экспрессия нормального количества рецепторов к ним на клетках. Изменение рецепторов после их связывания с цитокином заключается в интернализации комплексов цитокин — рецептор внутрь клетки. На поверхности клеток рецептор появляется заново, постепенно синтезируясь в течение 24-36 ч (время появления рецепторов интерферон-альфа). В этот период клетки остаются чувствительными к последующим дозам цитокина, чем объясняется эффективность введения препаратов интерферона и их индукторов три раза в неделю.
Пик продукции цитокинов после стимуляции макрофагов наблюдается через 1-2,6,18-48 ч, а пик продукции интерферон-гамма наступает через 20 ч после первого выхода цитокина из клетки. Поскольку интерферон-гамма ингибирует миелопоэз, то нормализация числа нейтрофилов после элиминации инфекта связана с системой регуляции нейтропоэза. Через 6 ч после стимуляции интерферон-альфа для выполнения своих функций NK-rклетки (активность которых регулируется ИЛ-1, 4, 2) продуцируют гамма-интерферон, в результате чего происходит лизис инфицированных клеток.
При антигенной стимуляции клеток трансдукция сигнала с активированного рецептора на генетический аппарат осуществляется с помощью внутриклеточных регуляторных систем, компоненты которых (белки мембран, ферментов, хроматина) связываются с чувствительными к ним последовательностями ДНК. После связывания цитокина (интерферон) с поверхностными клеточными мембранными рецепторами происходит активация ферментов протеинкиназы-С (ПКС), тирозинкиназы, ц-АМФзависимой протеинкиназы, серин-треонинкиназы. Интерферон-альфа активирует tyk 2 и jak 1-киназы, а интерферон-гамма активирует jak 1 и 2-киназы. Далее факторы транскрипции перемещаются в ядро клетки и связывают гены раннего ответа.
Первый ответ клеток на цитокин — это быстрая индукция генов раннего ответа («immediate early» генов), в число которых и входит ген интерферон-гамма. Стимуляция экспрессии этих генов важна для выхода клеток из Go-стадии и перехода в Gi-стадию и дальнейшей прогрессии клеточного цикла. Их индукция происходит после активации рецепторов роста на клеточной мембране и активации протеин-киназной системы. Гены раннего ответа являются ключевыми регуляторами клеточной пролиферации и дифференцировки, кодируют белки, регулирующие репликацию ДНК.
Таким образом, при активации клеток происходит стимуляция генов раннего ответа, что ассоциируется с изменением фаз клеточного цикла. Основная протективная роль в иммунном ответе, направленном против внутриклеточных паразитов (грибы, простейшие, вирусы, микобактерии туберкулеза), принадлежит клеточным механизмам. Способность перечисленных возбудителей переживать и размножаться внутри клеток делает их защищенными от действия антител и системы комплемента. Резистентность к антимикробным факторам макрофагов позволяет им длительно переживать внутри этих клеток. Для элиминации возбудителя необходим специфический клеточно-опосредованный ответ. Его специфичность определяется антигенраспознающими СД8+-Т-лимфоцитами, которые пролиферируют, активируются и формируют клон эффекторных цитотоксических лимфоцитов. Решающий момент специфического иммунного ответа — это ответ СД4+Т-лимфоцитов с хелперной направленностью на распознавание антигена. На этом этапе определяется форма иммунного ответа: либо с преобладанием гуморального иммунитета, либо с преобладанием клеточных реакций (ГЗТ). Направление дифференцировки СД4+-лимфоцитов, от которого зависит форма специфического иммунного ответа, контролируется цитокинами, образующимися в ходе воспалительной реакции. Так, в присутствии ИЛ-12 и интерферон-гамма СД4+-лимфоциты дифференцируются в воспалительные Тh1-клетки, начинают продуцировать и секретировать интерлейкин-2, интерферон-гамма, ФНО и определяют клеточный характер специфического иммунного ответа. Присутствие ИЛ-12 обеспечивается его продукцией макрофагами, а интерферон-гамма — естественными киллерами, активированными в раннюю фазу ответа на внутриклеточно паразитирующие бактерии и вирусы. В отличие от этого, в присутствии ИЛ-4 СД4+-лимфоциты дифференцируются в хелперы Тh 2, которые начинают продуцировать и секретировать ИЛ-4, ИЛ-5, ИЛ-6 и запускают гуморальный иммунный ответ, т.е. синтез специфических антител — иммуноглобулинов. Воспалительные Тh 1-лимфоциты нужны для борьбы с внутриклеточными паразитами, а Тh 2 хелперы нужны для элективной защиты от внеклеточных паразитов.
Вирусная инфекция может вызывать быстрое подавление экспрессии ряда клеточных генов (из которых наиболее изучены интерфероновые гены и гены, кодирующие дс-РНК-зависимые ферменты -2,5-ОАС и ПК-дс), принимающих участие в антивирусном действии. Специальные исследования механизма антивирусного действия интерферонов и дс-РНК в клеточных и бесклеточных системах показали ключевую роль в этом процессе вышеуказанных ферментов. ПК-дс, взаимодействуя с дс-РНК, фосфорилируется и в активной форме фосфорилирует регуляторные факторы транскрипции и трансляции, из которых наиболее изучен инициирующий фактор трансляции (eIF2).
ПК-дс выполняет регуляторную роль в системе клеточной пролиферации на уровне факторов трансляции и активации ряда генов цитокинов. Вероятно, существует связь между подавлением транскрипции мРНК и ПК-дс, угнетением общего синтеза клеточного белка при вирусных инфекциях и накоплением в ядрах клеток белка нуклеокапсида и белка NSP2. Фрагментация клеточных хромосом, наблюдающаяся на ранних сроках вирусной инфекции, может быть одной из причин подавления экспрессии генов, участвующих в противовирусном ответе.
Есть основания предполагать участие белков NSP2 в регуляции активности генов цитокинов — низкомолекулярных белковых регуляторных веществ, продуцируемых клетками и способных модулировать их функциональную активность. Нарушения в системе цитокинов приводят к нарушению кооперативных взаимодействий иммунокомпетентных клеток и нарушению иммунного гомеостаза.
В последние годы показано, что ИЛ- 12, относящийся к провоспалительным цитокинам, является ключевым для усиления клеточно-опосредованного иммунного ответа и инициации эффективной защиты против вирусов.
Средства терапии гриппа и ОРЗ можно разделить на этиотропные, иммунокорригирующие, патогенетические и симптоматические. Приоритет принадлежит этиотропным препаратам, действие которых направлено непосредственно на возбудитель инфекции. Все препараты этиотропного действия целесообразно рассматривать с учетом их точек приложения в цикле репродукции вирусов гриппа и других ОРЗ.
Применение химиопрепаратов для профилактики и лечения гриппа и ОРЗ относится к базовой терапии и является общепризнанным мировым стандартом. Многолетние клинические исследования достоверно выявили их высокую лечебно-профилактическую значимость. Химиотерапевтические средства представлены тремя основными группами: это блокаторы М2-каналов (амантадин, ремантадин); ингибиторы нейраминидазы (занамивир, озельтамивир) и ингибиторы протеаз (амбен, аминокапроновая кислота, трасилол). Препараты оказывают прямое антивирусное действие, нарушая различные фазы репликативного цикла вирусов. Несколько особняком стоит группа вирулицидных препаратов, применяемых местно для предотвращения адсорбции и проникновения вирионов в клетки.
СПИСОК ЛИТЕРАТУРЫ
- Грипп и другие респираторные вирусные инфекции / под ред. О.И. Киселева, И.Г. Мариничева, А.А. Сомининой. — СПб, 2003.
- Дриневский В.П., Осидак Л.В., Цыбалова Л.М. Острые респираторные инфекции у детей и подростков // Практическое руководство под редакцией О.И. Киселева. — СПб, 2003.
- Железникова Г.Ф., Иванова В.В., Монахова Н.Е. Варианты иммунопатогенеза острых инфекций у детей. СПб, 2007. — 254 с.
- Ершов Ф.И. Грипп и другие ОРВИ // Антивирусные препараты. Справочник. — М., 2006. — С.226-247.
- Ершов Ф.И., Романцов М.Г. Антивирусные средства в педиатрии. — М., 2005. — С.159-175.
- Ершов Ф.И., Киселев О.И. Интерфероны и их индукторы (от молекул до лекарств). М., 2005. — С.287-292.
- Иванова В.В. Острые респираторно-вирусные заболевания // Инфекционные болезни у детей. — М., 2002.
- Онищенко Г.Г., Киселев О.И., Соминина А.А. Усиление надзора и контроля за гриппом как важнейший элемент подготовки к сезонным эпидемиям и очередной пандемии. — М., 2004. — С.5-9.
- Об утверждении стандарта медицинской помощи больным гриппом, вызванным идентифицированным вирусом гриппа (грипп птиц) // Приказ Минздравсоцразвития №460 от 07.06.2006 г.
- Романцов М.Г., Ершов Ф.И.Часто болеющие дети: Современная фармакотерапия. — М., 2006. — 192 с.
- Стандартизированные принципы диагностики, лечения и экстренной профилактики гриппа и других острых респираторных инфекций у детей / под ред. О.И. Киселева. — Санкт-Петербург. — 2004. — С.82-95.
- Лекарственные средства в фармакотерапии патологии клетки / под ред. Т.Г.Кожока. — М., 2007.
Библиографическая ссылка
Сологуб Т.В., Ледванов М.Ю., Малый В.П., Стукова Н.Ю., Романцов М.Г., Бизенкова М.Н., Полякова Т.Д. ИММУННЫЙ ОТВЕТ ПРИ ВИРУСНЫХ ИНФЕКЦИЯХ // Успехи современного естествознания. – 2009. – № 12.
– С. 29-33;
URL: https://natural-sciences.ru/ru/article/view?id=14061 (дата обращения: 31.01.2023).
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
Резюме. Грипп является высококонтагиозной вирусной инфекцией и представляет собой серьезное бремя, особенно для детей в возрасте до 5 лет из-за повышенного риска тяжелого течения заболевания и госпитализации. Связанная с гриппом детская смертность в доковидный период регистрировалась ежегодно. Самый высокий уровень смертности регулярно регистрировался среди детей младшего возраста и особенно детей в возрасте до 6 месяцев. Доказано, что вакцинопрофилактика гриппа у детей младшего возраста безопасна и эффективна. Вакцинация против гриппа детей раннего возраста не только защищает эту уязвимую возрастную группу, но и является важным способом снижения передачи гриппа другим лицам из группы риска, а также сокращает использование медицинских услуг, включая применение антибиотиков. Иммунизация против гриппа в текущих эпидемиологических условиях особенно актуальна, поскольку в продолжающуюся пандемию COVID-19 невозможно предсказать интенсивность и сроки предстоящего сезонного подъема гриппа. Для профилактики гриппа у детей применяется любая лицензированная противогриппозная вакцина, соответствующая показаниям, однако в современных условиях приоритетом в профилактике гриппа является использование четырехвалентных вакцин, обеспечивающих развитие наиболее устойчивого иммунного ответа против ключевых штаммов вирусов гриппа. В четырехвалентные противогриппозные вакцины включены два штамма гриппа В линий Yamagata и Victoria в дополнение к штаммам гриппа A (H1N1 и H3N2). Исследования показали, что иммунизация четырехвалентной вакциной, в том числе детей раннего возраста, хорошо переносится и эффективно защищает от любых циркулирующих и антигенно совпадающих штаммов вирусов гриппа. Четырехвалентная инактивированная гриппозная вакцина российского производства полного цикла для профилактики сезонного гриппа – первая в Российской Федерации квадривакцина, одобренная к применению для иммунизации от гриппа детей с 6 месяцев и беременных. Вакцина соответствует всем рекомендациям Всемирной организации здравоохранения по составу и количеству гемагглютинина штамма вируса гриппа – содержит по 15 мкг гемагглютинина вируса гриппа каждого штамма (А(N1N1), A(N3N2), B линия Yamagata, B линия Victoria); не содержит иммуномодуляторов, адъювантов и консервантов; соответствует критериям иммуногенности для инактивированных гриппозных вакцин, принятых в Евросоюзе и Российской Федерации.
Вакцинация против гриппа (ВПГ) входит в Национальный календарь профилактических прививок РФ (утвержден Приказом Минздрава России от 06.12.2021 № 1122н) [1]. В соответствии с указанным документом возможность бесплатной вакцинации против гриппа имеют лица в возрасте 6 месяцев и старше. Это прежде всего категории граждан из перечисленных групп риска, которым ВПГ уменьшает шансы заболеть:
- дети с 6 месяцев до 18 лет;
- обучающиеся в профессиональных образовательных организациях и образовательных организациях высшего образования;
- беременные;
- взрослые старше 60 лет;
- пациенты с хроническими заболеваниями;
- взрослые, работающие по отдельным профессиям и должностям (сотрудники медицинских и образовательных организаций, транспорта, коммунальной сферы и сферы предоставления услуг); сотрудники правоохранительных органов и государственных контрольных органов в пунктах пропуска через государственную границу; работники организаций социального обслуживания и многофункциональных центров; государственные гражданские и муниципальные служащие;
- подлежащие призыву на военную службу;
- в 2021 г. добавилась новая категория – переболевшие COVID-19, поскольку, по данным исследований, грипп также опасен для них, поскольку реакция иммунной системы на инфицирование его вирусом может быть критичной [2].
В доковидный период число детей, ежегодно болевших острой респираторной вирусной инфекцией (ОРВИ), регистрировалось примерно на уровне 80-120 тыс. заболеваний на 100 тыс. населения детского возраста (что в 3,3-6 раз выше, чем у взрослых) и не имело тенденции к снижению [3]. При этом частота встречаемости зарегистрированных случаев гриппа у детей (в перерасчете на 100 тыс.) была в 1,9-2,8 раза выше, чем у всего населения. Спектр возбудителей ОРВИ был разным, обусловленным сезоном и возрастом: у дошкольников преобладали адено-, рино-, РС-, парагриппозный вирусы, у школьников – адено- и метапневмовирусы; в 25-30% случаев наблюдалось одновременное присутствие нескольких возбудителей (микст-инфекция). Вирусы гриппа доминировали у пациентов любого возраста во время эпидемического подъема этой инфекции.
К настоящему времени основной причиной заболеваемости и смертности от сезонного гриппа являются циркулирующие среди населения с конца 60-х годов прошлого столетия штаммы гриппа A(H3N2), за ними следуют штаммы гриппа B и штаммы A(H1N1). В начале 1980-х годов вирусы гриппа B разделились на две антигенно различные линии (B/Yamagata и B/Victoria) и в последние годы эти линии одновременно циркулируют по всему миру и вызывает эпидемии каждые 2-4 года [4].
Бремя гриппозной инфекции у детей раннего возраста значительно. Известно, что дети младше 5 лет, особенно младше 2 лет, и дети с определенными сопутствующими заболеваниями подвергаются повышенному риску госпитализации и осложнений [5, 6]. Около 10% госпитализированных младенцев и детей нуждаются в уходе в отделении интенсивной терапии, а некоторые даже ранее здоровые дети болеют крайне тяжело, в том числе и с летальным исходом [7, 8]. В допандемичный по COVID-19 период детская смертность, связанная с гриппом, регистрировалась ежегодно [9]. Самый высокий ее уровень регулярно регистрировался среди детей младшего возраста и особенно – в возрасте до 6 месяцев. Поэтому повышение уровня вакцинации детей, беременных и осуществляющих уход за младенцами может снизить детскую смертность, связанную с гриппом [10].
В эпидемиологическом сезоне 2020/2021 гг., совпавшем с пандемией новой коронавирусной инфекции (НКИ), вызванной распространением вируса SARS-CoV-2 по всему миру, заболеваемость гриппом практически не регистрировалась, что, возможно, было связано с высоким уровнем охвата вакцинацией, эпидемиологическими характеристиками респираторных вирусов во время пандемии, биологической конкуренцией между вирусами гриппа и SARS-CoV-2, а также строгими мерами контроля и защиты (ношение масок, дезинфекция, самоизоляция, соблюдение дистанции), направленными на предупреждение распространения инфекции [11]. Однако в завершившемся эпидсезоне 2021/2022 гг. эпидемиологическая ситуация полностью изменилась – распространение вирусов гриппа в России и мире значительно повысилось по сравнению с сезоном 2020/2021 гг. и его масштаб приблизился к уровню, наблюдавшемуся до пандемии COVID-19. В циркуляции наблюдалось абсолютное доминирование гриппа A(H3N2) и спорадическое выявление вирусов гриппа типа В и субтипа А(H1N1)pdm09. Обычно сезонный подъем заболеваемости гриппом фиксируется в декабре-январе, но в 2021 году первые случаи заболеваемости гриппом в России выявлялись лабораторно уже в августе и сентябре. Всего за два месяца осени 2021 г. ГНЦ ВБ «Вектор» полностью лабораторно подтвердил свыше 100 случаев гриппа А(Н3N2) в 18 субъектах РФ. За последние 10 лет впервые была зарегистрирована вспышечная заболеваемость гриппом в столь ранние сроки [12].
В этом году ситуация может оказаться серьезнее, так как ожидается циркуляция нового вируса гриппа подтипа A(N3N2) – А /Darwin/9/2021 и вируса типа В линии Victoria В/ Austria/1359417/2021, раньше в популяции они не встречались, а иммунитет к ним у населения отсутствует. Кроме того, в мире продолжают циркулировать штаммы вируса гриппа, подобные тому, который вызвал пандемию в 2009-2010 годах, – A(N3N2) – А/Darwin/9/2021 (свиной грипп). Он считается одним из опасных, так как может вызывать вирусную пневмонию и довольно тяжелое течение болезни [13].
Поэтому штаммовый состав вакцин для начавшегося нового сезона 2022/2023 гг. существенно изменился – в трехвалентной вакцине заменены два штамма из трех, включенных в вакцину предыдущего сезона, в четырехвалентной — два штамма (табл.). В обновленный состав вакцин, согласно рекомендациям Всемирной организации здравоохранения (ВОЗ) для стран Северного полушария, включены антигены штаммов вирусов, которые ожидаются в предстоящем эпидемическом сезоне: A(N3N2) – А/Darwin/9/2021 и В линии Victoria В/Austria/1359417/2021, антиген вируса А(Н1N1)pdm09 – А/Victoria/2570/2019 остался неизменным [14].

Постановлением Главного государственного санитарного врача РФ в сезоне 2022/2023 гг. рекомендовано достичь охвата иммунизацией против гриппа не менее 60% от численности населения страны и не менее 75% входящих в группы риска, предусмотренные Национальным календарем, что позволит снизить заболеваемость, долю тяжелых случаев гриппа и число осложнений, связанных с этим заболеванием, что также уменьшит нагрузку на лечебную сеть в период эпидемического подъема заболеваемости [15].
Несмотря на то, что всеобщая и ежегодная вакцинация против гриппа рекомендуется всем начиная с 6 месяцев, особое внимание следует уделить охвату ею детей из групп высокого риска и уязвимых по состоянию здоровья пациентов, а также контактирующих с ними в семье и опекунов.
В состав современных вакцин против гриппа, применяемых на территории РФ для иммунизации населения, входят только фрагменты генетического материала рекомендованных ВОЗ штаммов вирусов гриппа A(N1N1), A(N3N2) и В, поэтому вакцины не могут вызвать гриппозную инфекцию. Но этих коротких участков генома вирусов достаточно, чтобы в организме человека сформировался иммунный ответ [16].
Вакцинация современными противогриппозными вакцинами безопасна и для страдающих аллергическими заболеваниями, что особенно актуально для детей, в т. ч. раннего возраста [17]. Интернациональный консенсус «Аллергия и вакцинация» (International Consensus (ICON): allergic reactions to vaccines, 2016), основываясь на рекомендации ведущих экспертов международных аллергологических сообществ, констатирует, что ВПГ абсолютно безопасна для имеющих указание в анамнезе на аллергию к куриному белку [18]. Предварительное аллергологическое тестирование на определение специфических IgE, а также кожное тестирование непосредственно перед вакцинацией не требуются. Единственным абсолютным противопоказанием для ее проведения является острая аллергическая реакция на предыдущее введение вакцины [18, 19].
Международные исследования подтвердили эффективность иммунизации детей раннего возраста против гриппа. Так, проведенное в Японии исследование показало, что эффективность ВПГ у детей от 6 месяцев до 6 лет составляет от 42% до 69% в зависимости от соответствия вакцинных штаммов циркулирующим в эпидсезон вирусам; по оценкам этого же исследования, вакцинопрофилактика снижает частоту госпитализаций, связанных как с гриппом типа A, так и с гриппом типа B [20].
В последние годы опубликовано несколько рандомизированных клинических исследований (РКИ) с участием детей от 6 месяцев до 4 лет [21-25], представивших данные о том, что ВПГ эффективна у детей младшего возраста с результатами в диапазоне от 25,6% (95% ДИ 6,8-40,6) до 87% (95% ДИ 0,0-98,0) по разным публикациям. Кроме того, многоцентровое 5-летнее исследование эффективности противогриппозных вакцин у детей в возрасте 6-35 месяцев продемонстрировало сокращение использования медицинских услуг, включая применение антибиотиков [21].
Результаты когортных исследований, проведенных странах, где действуют программы всеобщей вакцинации, включающие детей в возрасте от 6 месяцев, с целью оценки влияния специфической иммунизации на профилактику гриппа, также показывают, что эффективность ВПГ в этой возрастной группе оказывается значительной [26-28].
Обзор обсервационных исследований (несмотря на то, что к ним следует относиться с осторожностью, поскольку, учитывая характер типов исследований, существует значительный риск систематической ошибки) также демонстрирует эффективность противогриппозной вакцины у детей, в т. ч. раннего возраста [29-31].
Все исследования последних лет, проведенные в разных регионах мира, продемонстрировали относительно высокую эффективность и безопасность ВПГ детей, в том числе в возрасте до 2 лет, а также с риском тяжелого заболевания [32].
Одним из косвенных способов защиты уязвимых групп населения, таких как младенцы до 6 месяцев, люди с ослаб-ленной иммунной системой и пожилые, является увеличение охвата детей ВПГ. Известно, что дети играют важную эпидемиологическую роль в распространении гриппа, поскольку они находятся в тесном контакте друг с другом в детских учреждениях и школах, тесно контактируют со взрослыми и пожилыми людьми в семьях, имеют недостаточно сформированные гигиенические привычки и ограниченный приобретенный иммунитет. Кроме того, дети выделяют высокие титры вируса и более длительно (10-15 дней), чем взрослые и пожилые люди, становясь «суперраспространителями» сезонных эпидемий гриппа. Показано, что программы ВПГ для детей значительно снижают заболеваемость гриппом и смертность среди пожилых, а также уровень гриппоподобных заболеваний у детей [33, 34].
Имеются убедительные доказательства того, что ВПГ детей обеспечивает косвенную защиту непривитых лиц на уровне семей и населения в целом [35]. ВПГ является важной стратегией защиты детей и всего общества, а также снижения общего бремени респираторных заболеваний, когда другие вирусы, в том числе новый коронавирус SARS-CoV-2, циркулируют одновременно [36]. Любая лицензированная противогриппозная вакцина, соответствующая возрасту и состоянию здоровья, может быть введена, в идеале, как можно скорее в течение сезона, без предпочтения одного продукта или состава другому [37]. Недавний отчет японского педиатрического общества, включавший сведения о 29 400 детях (9347, 4435 и 15 618 с гриппом А и В и с отрицательным результатом соответственно), показал, что в течение последних семи сезонов, непосредственно предшествовавших пандемии COVID-19, инактивированные противогриппозные вакцины были эффективны как против гриппа А, так и против гриппа В во всех возрастных группах детей, за исключением гриппа В у детей 6-11 месяцев (возможно, из-за незрелости иммунной системы младенцев в этом возрасте, а также активной циркуляции в последние годы до текущей пандемии НКИ нескольких штаммов вируса гриппа В). В то же время эффективность иммунизации была самой высокой среди детей в возрасте 1-2 лет как при гриппе А, так и при гриппе В. Представленные в отчете данные свидетельствуют также о том, что вакцинация эффективно снижает частоту госпитализации детей от 1 года до 12 лет с гриппом А [36].
Для иммунизации населения против гриппа многие годы применяли трехвалентную вакцину, содержащую два штамма гриппа А (H1N1 и H3N2) и один штамм В. Поскольку в трехвалентные противогриппозные вакцины включают штамм только одной выбранной линии вирусов гриппа B, то они могут обеспечивать ограниченный иммунитет против штаммов другой линии этого типа, следовательно, могут иметь сниженную эффективность в те сезоны, когда значительная часть эпидемии гриппозной инфекции вызывается не вошедшими в состав вакцины штаммами типа B. В четырехвалентные противогриппозные вакцины включены два штамма гриппа В линий Yamagata и Victoria B в дополнение к штаммам гриппа A (H1N1 и H3N2), что позволяет обеспечить более широкую защиту [38].
В РФ в последние годы в рамках Национального календаря профилактических прививок применяли отечественные трехвалентные противогриппозные вакцины Ультрикс®, Гриппол® плюс, Совигрипп®, ФлюМ®. С 2017 г. отечественные вакцины Ультрикс®, Гриппол® плюс, Совигрипп® рекомендованы детям начиная с 6-месячного возраста, а также беременным. Вакцины для детских возрастных групп не содержат консерванта.
Поскольку эпидемическая ситуация по гриппу в последние годы характеризуется одновременной циркуляцией всех 4 штаммов вирусов гриппа (подтипов H1N1 и H3N2 гриппа типа А и обеих линий Yamagata и Victoria гриппа типа В), каждый из которых может вызвать заболевание, предпочтительной становится четырехвалентная (квадривалентная) вакцина, обеспечивающая большую защиту, такой препарат уже доступен для вакцинации и в РФ. В 2019 г. была зарегистрирована первая четырехвалентная инактивированная гриппозная вакцина российского производства полного цикла Ультрикс® Квадри, которая полностью соответствует рекомендациям ВОЗ и содержит по два антигена вируса гриппа типа А – подтипы А(H1N1) и А(H3N2) и типа B (линии Yamagata и линии Victoria) [39]. В состав вакцины входит 15 мкг гемагглютинина каждого штамма в одной дозе, всего в одной дозе содержится 60 мкг антигенов. Показания к применению вакцины Ультрикс® Квадри – активная ежегодная профилактическая иммунизация против сезонного гриппа детей с 6-месячного возраста, подростков и взрослых без ограничения возраста [40]. Четырехвалентная вакцина Ультрикс® Квадри стала первой в России, одобренной к применению для иммунизации от гриппа детей с 6 месяцев и беременных. Показано, что массовый переход на более эффективную четырехвалентную вакцину против гриппа экономически целесообразен [41]. Результаты РКИ, опубликованные недавно итальянскими педиатрами, показали, что иммунизация квадривалентной вакциной детей 6-35 месяцев хорошо переносится и эффективно защищает от любых циркулирующих и антигенно совпадающих штаммов вирусов гриппа: 54% (95% ДИ 37,0-6,0) и 68% (95% ДИ 45,0-81,0) соответственно) [42]. Выраженные и стойкие серологические реакции, продемонстрированные в этом исследовании, включая выработку антител против гемагглютинина, нейраминидазы и нейтрализующих антител, свидетельствуют о том, что квадривалентная вакцина может обеспечивать устойчивый иммунный ответ против ключевых штаммов вирусов гриппа, вызывающих высокую заболеваемость у детей раннего возраста.
Союз педиатров России и Американская академия педиатрии рекомендуют проводить ежегодную ВПГ всех детей без медицинских противопоказаний начиная с 6-месячного возраста [37, 43].
Ультрикс Квадри, в соответствии с инструкцией используется у детей с 6 месяцев до 3 лет двукратно 0,25 мл, если ребенок не боле гриппом.
Беременные могут получить вакцину против гриппа на любом сроке гестации, чтобы защитить себя и своих детей. Вакцинация против гриппа во время грудного вскармливания безопасна для матерей и их детей.
Таким образом, в современных эпидемиологических условиях продолжающейся пандемии и ожидания в осенние месяцы сезонного подъем заболеваемости гриппом и другими ОРВИ особенно актуальной становится проведение в максимально короткие сроки ВПГ населения, а также сохранение в полном объеме плановой вакцинации детей в рамках Национального календаря прививок. Дети, которым показана вакцинация против COVID-19, могут получить ее одновременно с вакцинацией против гриппа в одно и то же посещение. ВПГ недоношенным проводится в соответствии с сезоном, когда они достигают 6-месячного возраста. Врачам, медсестрам и членам семьи, окружающим недоношенного ребенка, которому не исполнилось 6 месяцев, рекомендуется пройти вакцинацию, чтобы снизить вероятность заражения ребенка гриппом. Антитела и клеточные иммунные ответы на вакцину против гриппа у недоношенных вырабатываются в значительно более низких титрах, чем у доношенных в возрасте от 6 месяцев до 4 лет. Тем не менее исследования показали, что почти у всех младенцев формируется средний геометрический уровень титра антител > 1:32 (уровень, который, как считается, коррелирует с защитой) независимо от гестационного возраста [44].
Необходимость ВПГ детей в текущих эпидемиологических условиях имеет особенно веские причины.
Во-первых, во время пандемии COVID-19 невозможно предсказать сроки и интенсивность предстоящих сезонов гриппа. Во-вторых, теоретически иммунитет к вирусам гриппа, вероятно, ослабел из-за низкой активности гриппа в 2020 году, особенно среди детей раннего возраста, которые еще не были иммунизированы или не подвергались естественному контакту с вирусом гриппа. В результате может возникнуть отсроченная или несвоевременная эпидемия гриппа, как это наблюдалось при прошлогодней эпидемии, вызванной респираторно-синцитиальным вирусом (РСВ). После низкой заболеваемости РСВ-инфекцией в 2020 году во время пандемии COVID-19 повсеместно в мире отмечался рост числа госпитализированных детей весной/летом 2021 года, когда меры общественного контроля были ослаблены и произошел возврат к социальной активности [45, 46]. В-третьих, недавние публикации показали, что иммунизация противогриппозной вакциной связана с уменьшением симптомов и смертности среди пациентов с COVID-19, включая детей, возможно, благодаря неспецифической активации врожденных иммунных реакций и, например, посредством такого механизма, как вирусная интерференция, вызванная вакциной, что требует дальнейшего изучения [47-49].
Для профилактики гриппа у детей применяется любая лицензированная противогриппозная вакцина, соответствующая показаниям, однако представляется целесообразным использование квадривалентных вакцин, содержащих как два штамма гриппа А, так и два штамма гриппа В. Ультрикс Квадри – первая российская четырехвалентная вакцина для профилактики сезонного гриппа, отвечающая всем рекомендациям ВОЗ по составу и количеству гемагглютинина штамма вируса гриппа [50], – содержит по 15 мкг гемагглютинина вируса гриппа каждого штамма (A/H1N1, A/H3N2, B линия Yamagata, B линия Victoria); не содержит адъювантов, стабилизаторов и консервантов; соответствует критериям иммуногенности для инактивированных гриппозных вакцин, принятых в Евросоюзе и РФ; одобрена для применения у беременных и детей с 6 месяцев.
КОНФЛИКТ ИНТЕРЕСОВ. Авторы статьи подтвердили отсутствие конфликта интересов, о котором необходимо сообщить.
CONFLICT OF INTERESTS. Not declared.
Литература/References
- Приказ Министерства здравоохранения Российской Федерации от 06.12.2021 № 1122н «Об утверждении национального календаря профилактических прививок, календаря профилактических прививок по эпидемическим показаниям и порядка проведения профилактических прививок» (Зарегистрирован 20.12.2021 № 66435) [Order of the Ministry of Health of the Russian Federation dated December 6, 2021 No. 1122n «On approval of the national calendar of preventive vaccinations, the calendar of preventive vaccinations for epidemic indications and the procedure for conducting preventive vaccinations» (Registered on December 20, 2021 No. 66435) (in Russ.)]
- Пшеничная Н. Ю., Карева Е. Н., Ленева И. А., и др. Фармакоэпидемиологическое исследование COVID-19 в Российской Федерации ЭГИДА-2020 // Терапевтический архив. 2021; 93 (11): 1306-1315. DOI: 10.26442/00403660.2021.11.201206 [Pshenichnaya N. Y., Kareva E. N., Leneva I. A., et al. Pharmacoepidemiological research of COVID-19 in the Russian Federation EGIDA-2020 // Terapevticheskii arkhiv. 2021; 93 (11): 1306-1315. (in Russ.) DOI: 10.26442/00403660.2021.11.201206]
- Сведения об инфекционных и паразитарных заболеваниях за январь—декабрь 2018 в РФ // Детские инфекции. 2019; 18 (1): 5. [Data on infectious and parasitic diseases for January-December 2018 in the Russian Federation. Children’s infections. 2019; 18(1):5. (in Russ.)]
- Caini S., Kusznierz G., Garate V. V., et al. The epidemiological signature of influenza B virus and its B/Victoria and B/Yamagata lineages in the 21st century // PLoS One. 2019 Sep 12; 14 (9): e0222381. DOI: 10.1371/journal.pone.0222381
- Gill P. J., Ashdown H. F., Wang K., et al. Identification of children at risk of severe influenza-related complications in primary and ambulatory care: a systematic review and meta-analysis // Lancet Respir Med. 2014; (published online Dec 4.) http://dx.doi.org/10.1016/S2213-2600(14)70252-8
- Булгакова В. А., Поромов А. А., Грекова А. И., и др. Фармакоэпидемио-логическое исследование течения гриппа и других ОРВИ в группах риска // Терапевтический архив. 2017;89 (1): 62-71. DOI: 10.17116/terarkh201789162-71 [Bulgakova V. A., Poromov A. A., Grekova A. I., et al. Pharmacoepidemiological study of the course of influenza and other acute respiratory viral infections in risk groups // Terapevticheskii arkhiv. 2017; 89 (1): 62-71 (in Russ.) DOI: 10.17116/terarkh201789162-71]
- Hauge S. H., de Blasio B. F., Håberg S. E., Oakley L. Influenza hospitalizations during childhood in children born preterm // Influenza Other Respir Viruses. 2022 Mar; 16 (2): 247-254. DOI: 10.1111/irv.12908
- Учайкин В. Ф., Шамшева О. В., Молочкова О. В., Булгакова В. А. Фармако-эпидемиологическое исследование течения гриппа и других ОРВИ в сезоне 2010/11 гг. у детей в возрасте до 18 лет // Детские инфекции. 2016; 11 (S): 9-15. [Uchaikin V. F., Shamsheva O. V., Molochkova O. V., Bulgakova V. A. Pharmacological and Epidemiological Study of the Course of Influenza and Other ARVI in the Season 2010/11 in Children under the Age of 18 // Children’s infections. 2016; 11 (S): 9-15. (in Russ.)]
- Shang M., Blanton L., Brammer L., Olsen S. J., Fry A. M. Influenza-Associated Pediatric Deaths in the United States, 2010-2016 // Pediatrics. 2018 Apr; 141 (4): e20172918. DOI: 10.1542/peds.2017-2918
- Nair H., Widdowson M. A. Paediatric influenza vaccination: time to better protect high-risk groups? // Lancet Respir Med. 2015 Feb; 3 (2): 93-94. DOI: 10.1016/S2213-2600(14)70285-1
- Han X., Xu P., Wang H., Mao J., Ye Q. Incident changes in the prevalence of respiratory virus among children during COVID-19 pandemic in Hangzhou, China // J Infect. 2022 Apr; 84 (4): 579-613. DOI: 10.1016/j.jinf.2022.01.007
- https://www.rospotrebnadzor.ru/about/info/news/news_details.php?ELEMENT_ID=19389
- Галкина С. Н., Осидак Л. В., Волощук Л. В. и др. Ранние поражения легких при гриппе // Детские инфекции. 2017; 16 (2): 13-22. [Galkina S. N., Osidak L. V., Voloshchuk L. V., еt al. Early lung lesions in influenza // Children’s infections. 2017;16 (2): 13-22 (in Russ.)]
- World Health Organization. Recommended composition of influenza virus vaccines for use in the 2022-2023 northern hemisphere influenza season. Available at: https://www.who.int/publications/m/item/recommended-composition- of-influenza-virus-vaccines-for-use-in- the-2022-2023-northern-hemisphere- influenza-season. Accessed 19 Sep. 2022.
- Постановление Главного государственного санитарного врача Российской Федерации от 28.07.2022 № 20 «О мероприятиях по профилактике гриппа и острых респираторных вирусных инфекций в эпидемическом сезоне 2022-2023 годов» (Зарегистрирован 22.08.2022 № 69712)
- Гендон Ю. З. Вакцины и химиопрепараты для профилактики гриппа // Вопросы вирусологии. 2007; 52 (1): 4-10. [Gendon Yu. Z. Vaccines and chemotherapy drugs for the prevention of influenza // Issues of Virology. 2007; 52 (1): 4-10. (in Russ.)]
- Bulgakova V., Balabolkin I., Eliseeva T., Yusupova D. Influenza vaccination of children with atopic bronchial asthma. Allergy. 2017. 72 (S103): 361.
- Dreskin S. C., Halsey N. A., Kelso J. M., et al. International Consensus (ICON): allergic reactions to vaccines // World Allergy Organ J. 2016 Sep 16; 9 (1): 32. DOI: 10.1186/s40413-016-0120-5
- Echeverría-Zudaire L. A., Ortigosa-del Castillo L., Alonso-Lebrero E., et al. Consensus document on the approach to children with allergic reactions after vaccination or allergy to vaccine components. Allergol Immunopathol (Madr). 2015 May-Jun;43 (3): 304-325. DOI: 10.1016/j.aller.2015.01.004
- Katayose M., Hosoya M., Haneda T., Yamaguchi H., Kawasaki Y., Sato M., Wright P. F. The effectiveness of trivalent inactivated influenza vaccine in children over six consecutive influenza seasons // Vaccine. 2011 Feb 17; 29 (9): 1844-9. DOI: 10.1016/j.vaccine.2010.12.049
- Pepin S., Dupuy M., Borja-Tabora C. F. C., et al. Efficacy, immunogenicity, and safety of a quadrivalent inactivated influenza vaccine in children aged 6-35 months: A multi-season randomised placebo-controlled trial in the Northern and Southern Hemispheres // Vaccine. 2019 Mar 22; 37 (13): 1876-1884. DOI: 10.1016/j.vaccine.2018.11.074
- Claeys C., Zaman K., Dbaibo G., et al. Prevention of vaccine-matched and mismatched influenza in children aged 6-35 months: a multinational randomised trial across five influenza seasons // Lancet Child Adolesc Health. 2018 May;.2.(5):.338-349. DOI: 10.1016/S2352-4642(18)30062-2
- Dbaibo G., Amanullah A., Claeys C., et al. Quadrivalent Influenza Vaccine Prevents Illness and Reduces Healthcare Utilization Across Diverse Geographic Regions During Five Influenza Seasons: A Randomized Clinical Trial // Pediatr Infect Dis J. 2020 Jan; 39 (1): e1-e10. DOI: 10.1097/INF.0000000000002504
- Rolfes M. A., Goswami D., Sharmeen A. T., et al. Efficacy of trivalent influenza vaccine against laboratory-confirmed influenza among young children in a randomized trial in Bangladesh // Vaccine. 2017 Dec 15; 35 (50): 6967-6976. DOI: 10.1016/j.vaccine.2017.10.074
- Li-Kim-Moy J. P., Yin J. K., Heron L., et al. Influenza vaccine efficacy in young children attending childcare: A randomised controlled trial // J Paediatr Child Health. 2017 Jan; 53 (1): 47-54. DOI: 10.1111/jpc.13313
- Buchan S. A., Chung H., Campitelli M. A., et al. Vaccine effectiveness against laboratory-confirmed influenza hospitalizations among young children during the 2010-11 to 2013-14 influenza seasons in Ontario, Canada // PLoS One. 2017 Nov 17; 12 (11): e0187834. DOI: 10.1371/journal.pone.0187834
- Blyth C. C., Macartney K. K., McRae J., et al. Influenza Epidemiology, Vaccine Coverage and Vaccine Effectiveness in Children Admitted to Sentinel Australian Hospitals in 2017: Results from the PAEDS-FluCAN Collaboration // Clin Infect Dis. 2019 Mar 5; 68 (6): 940-948. DOI: 10.1093/cid/ciy597
- Blyth C. C., Jacoby P., Effler P. V., et al. Effectiveness of trivalent flu vaccine in healthy young children. Pediatrics. 2014 May;133 (5): e1218-25. DOI: 10.1542/peds.2013-3707
- Simpson C. R., Lone N. I., Kavanagh K., et al. Vaccine effectiveness of live attenuated and trivalent inactivated influenza vaccination in 2010/11 to 2015/16: the SIVE II record linkage study // Health Technol Assess. 2020 Dec; 24 (67): 1-66. DOI: 10.3310/hta24670
- Jackson M. L., Chung J. R., Jackson L. A., et al. Influenza Vaccine Effectiveness in the United States during the 2015-2016 Season // N Engl J Med. 2017 Aug 10; 377 (6): 534-543. DOI: 10.1056/NEJMoa1700153
- Pebody R. G., Whitaker H., Ellis J., et al. End of season influenza vaccine effectiveness in primary care in adults and children in the United Kingdom in 2018/19 // Vaccine. 2020 Jan 16; 38 (3): 489-497. DOI: 10.1016/j.vaccine.2019.10.071
- Bansal A., Trieu M. C., Mohn K. G. I., Cox R. J. Safety, Immunogenicity, Efficacy and Effectiveness of Inactivated Influenza Vaccines in Healthy Pregnant Women and Children Under 5 Years: An Evidence-Based Clinical Review // Front Immunol. 2021 Oct 6; 12: 744774. DOI: 10.3389/fimmu.2021.744774
- Sugaya N., Takeuchi Y. Mass vaccination of schoolchildren against influenza and its impact on the influenza-associated mortality rate among children in Japan // Clin Infect Dis. 2005 Oct 1; 1 (7): 939-47. DOI: 10.1086/432938
- Ghendon Y. Z., Kaira A. N., Elshina G. A. The effect of mass influenza immunization in children on the morbidity of the unvaccinated elderly // Epidemiol Infect. 2006 Feb; 134 (1): 71-8. DOI: 10.1017/S0950268805005650
- Yin J. K., Heywood A. E., Georgousakis M., et al. Systematic Review and Meta-analysis of Indirect Protection Afforded by Vaccinating Children Against Seasonal Influenza: Implications for Policy // Clin Infect Dis. 2017 Sep 1; 65 (5): 719-728. DOI: 10.1093/cid/cix420. PMID: 28475770
- Shinjoh M., Furuichi M., Kobayashi H., et al. Trends in effectiveness of inactivated influenza vaccine in children by age groups in seven seasons immediately before the COVID-19 era // Vaccine. 2022 May 11; 40 (22): 3018-3026. DOI: 10.1016/j.vaccine.2022.04.033
- Recommendations for Prevention and Control of Influenza in Children, 2022-2023 // Pediatrics. 2022 Sep 6: e2022059274. DOI: 10.1542/peds.2022-059274
- Ambrose C. S., Levin M. J. The rationale for quadrivalent influenza vaccines. Hum Vaccin Immunother. 2012 Jan; 8 (1): 81-88. DOI: 10.4161/hv.8.1.17623
- Булгакова В. А., Селимзянова Л. Р., Чемакина Д. С., Привалова Т. Е. Вакцинация против гриппа у детей – как обстоят дела в текущем сезоне // Лечащий Врач. 2020; (5): 54. https://doi.org/10.26295/OS.2020.58.32.010 [Bulgakova V. A., Selimzyanova L. R., Chemakina D. S., Privalova T. E. Vaccination against influenza in children – how it goes this season // Lechaschi Vrach. 2020; (5): 54. (in Russ.) https://doi.org/10.26295/OS.2020.58.32.010]
- Инструкции по медицинскому применению лекарственного препарата Ультрикс® Квадри. https://grls.rosminzdrav.ru/Grls_View_v2.aspx?routingGuid=ba510c96-6598-4619-996a-0c3d6f4ee78d&t [Instructions for the medical use of the drug Ultrix® Quadri. https://grls.rosminzdrav.ru/Grls_View_v2.aspx?routingGuid=ba510c96-6598-4619-996a-0c3d6f4ee78d&t]
- Усков А. А., Шипилов М. В., Тутельян А. В. Фармакоэкономическое обоснование использования четырехвалентной вакцины против гриппа в Российской Федерации // Инфекционные болезни. 2020; 18 (1): 96-101. DOI: 10.20953/1729-9225-2020-1-96-101 [Uskov A. A., Shipilov M. V., Tutelyan A. V. Pharmacoeconomic analysis of using a quadrivalent influenza vaccine in the Russian Federation // Infekts. bolezni (Infectious diseases). 2020; 18 (1): 96-101. (in Russ.) DOI: 10.20953/1729-9225-2020-1-96-101]
- Esposito S., Nauta J., Lapini G., Montomoli E., van de Witte S. Efficacy and safety of a quadrivalent influenza vaccine in children aged 6-35 months: A global, multiseasonal, controlled, randomized Phase III study // Vaccine. 2022 Apr 20; 40 (18): 2626-2634. DOI: 10.1016/j.vaccine.2022.02.088
- Прикладные аспекты иммунопрофилактики гриппа у детей и взрослых в период пандемии COVID-19 // Педиатрическая фармакология. 2020; 17 (6): 575-576. [Applied features of influenza immunoprophylaxis in children and adults during covid-19 pandemic // Pediatric pharmacology. 2020; 17 (6): 575-576. (In Russ.)]
- Gagneur A., Pinquier D., Quach C. Immunization of preterm infants. Hum Vaccin Immunother 2015; 11 (11): 2556-2563. DOI: 10.1080/21645515.2015.1074358
- Weinberger Opek M., Yeshayahu Y., Glatman-Freedman A., et al. Delayed respiratory syncytial virus epidemic in children after relaxation of COVID-19 physical distancing measures, Ashdod, Israel, 2021 // Euro Surveill. 2021 Jul; 26(29): 2100706. DOI: 10.2807/1560-7917.ES.2021.26.29.2100706
- Ujiie M., Tsuzuki S., Nakamoto T., Iwamoto N. Resurgence of Respiratory Syncytial Virus Infections during COVID-19 Pandemic, Tokyo, Japan // Emerg Infect Dis. 2021 Nov; 27 (11): 2969-2970. DOI: 10.3201/eid2711.211565
- Patwardhan A., Ohler A. The Flu Vaccination May Have a Protective Effect on the Course of COVID-19 in the Pediatric Population: When Does Severe Acute Respiratory Syndrome Coronavirus 2 (SARS-CoV-2) Meet Influenza? // Cureus. 2021 Jan 6; 13 (1): e12533. DOI: 10.7759/cureus.12533
- Kowalska M., Niewiadomska E., Baranski K., et al. Association between Influenza Vaccination and Positive SARS-CoV-2 IgG and IgM Tests in the General Population of Katowice Region, Poland // Vaccines (Basel). 2021 Apr 21; 9 (5): 415. DOI: 10.3390/vaccines9050415
- Fink G., Orlova-Fink N., Schindler T., et al. Inactivated trivalent influenza vaccination is associated with lower mortality among patients with COVID-19 in Brazil // BMJ Evid Based Med. 2020 Dec 11: bmjebm-2020-111549. DOI: 10.1136/bmjebm-2020-111549
- Резолюция XX Конгресса педиатров России с международным участием «Актуальные проблемы педиатрии». Педиатрическая фармакология. 2018; 15(2): 191-192. [Resolution of the XX Congress of Russian Pediatricians with International Participation «Actual Problems of Pediatrics». Pediatric pharmacology. 2018; 15 (2): 191-192. (In Russ.)]
В. А. Булгакова1, 2, ORCID: 0000-0003-4861-0919, irvilbulgak@mail.ru
Л. Р. Селимзянова1-3, ORCID: 0000-0002-3678-7939, lilysir@mail.ru
Т. Е. Привалова1, 2, ORCID: 0000-0003-4680-2925, privalova-tatyana@yandex.ru
Д. А. Юсупова4, ORCID: 0000-0002-6822-5383, dilyara.yus1997@mail.ru
1 Научно-исследовательский институт педиатрии и охраны здоровья детей, Научно-клинический центр № 2 Федерального государственного бюджетного научного учреждения Российский научный центр хирургии имени академика Б. В. Петровского; 119333, Россия, Москва, ул. Фотиевой, 10, стр. 1
2 Федеральное государственное автономное образовательное учреждение высшего образования Российский национальный исследовательский медицинский университет имени Н. И. Пирогова Министерства здравоохранения Российской Федерации; 117997, Россия, Москва, ул. Островитянова, 1
3 Академия постдипломного образования Федерального государственного бюджетного учреждения Федеральный научно-клинический центр Федерального медико-биологического агентства России; 125310, Россия, Москва, Волоколамское шоссе, 91
4 Акционерное общество «Международный биотехнологический центр «Генериум»; 601125, Россия, Владимирская область, Петушинский район, поселок Вольгинский, ул. Заводская, стр. 273
Сведения об авторах:
Булгакова Виля Ахтямовна, д.м.н., заведующая отделом научно-информационного развития Научно-исследовательского института педиатрии и охраны здоровья детей, Научно-клинический центр № 2 Федерального государственного бюджетного научного учреждения Российский научный центр хирургии имени академика Б. В. Петровского; 119333, Россия, Москва, ул. Фотиевой, 10, стр. 1; профессор кафедры факультетской педиатрии педиатрического факультета Федерального государственного автономного образовательного учреждения высшего образования Российский национальный исследовательский медицинский университет имени Н. И. Пирогова Министерства здравоохранения Российской Федерации; 117997, Россия, Москва, ул. Островитянова, 1; irvilbulgak@mail.ru
Селимзянова Лилия Робертовна, к.м.н., заведующая отделом стандартизации и изучения основ доказательной медицины Научно-исследовательского института педиатрии и охраны здоровья детей, Научно-клинический центр № 2 Федерального государственного бюджетного научного учреждения Российский научный центр хирургии имени академика Б. В. Петровского; 119333, Россия, Москва, ул. Фотиевой, 10, стр. 1; доцент кафедры факультетской педиатрии педиатрического факультета Федерального государственного автономного образовательного учреждения высшего образования Российский национальный исследовательский медицинский университет имени Н. И. Пирогова Министерства здравоохранения Российской Федерации; 117997, Россия, Москва, ул. Островитянова, 1; ассистент кафедры педиатрии Академии постдипломного образования Федерального государственного бюджетного учреждения Федеральный научно-клинический центр Федерального медико-биологического агентства России; 125310, Россия, Москва, Волоколамское шоссе, 91; lilysir@mail.ru
Привалова Татьяна Евгеньевна, к.м.н., доцент кафедры факультетской педиатрии педиатрического факультета Федерального государственного автономного образовательного учреждения высшего образования Российский национальный исследовательский медицинский университет имени Н. И. Пирогова Министерства здравоохранения Российской Федерации; 117997, Россия, Москва, ул. Островитянова, 1; ведущий научный сотрудник отдела разработки научных подходов к иммунизации пациентов с отклонениями в состоянии здоровья и хроническими болезнями Научно-исследовательского института педиатрии и охраны здоровья детей, Научно-клинический центр № 2 Федерального государственного бюджетного научного учреждения Российский научный центр хирургии имени академика Б. В. Петровского; 119333, Россия, Москва, ул. Фотиевой, 10, стр. 1; privalova-tatyana@yandex.ru
Юсупова Диляра Ахметовна; сотрудник Акционерного общества «Международный биотехнологический центр «Генериум»; 601125, Россия, Владимирская область, Петушинский район, поселок Вольгинский, ул. Заводская, стр. 273; dilyara.yus1997@mail.ru
Information about the authors:
Vilya A. Bulgakova, Dr. of Sci. (Med.), Head of the Department of Scientific and Information Development at the Scientific Research Institute of Pediatrics and Child Research Institute, Scientific and Clinical Center No. 2 of the Federal State Budgetary Scientific Institution Petrovsky National Research Centre of Surgery, 10 b. 1 Fotieva str., Moscow, 119333, Russia; Professor of the Department of Faculty Pediatrics of the Pediatric Faculty at the Federal State Autonomous Educational Institution of Higher Education N. I. Pirogov Russian National Research Medical University of the Ministry of Health of the Russian Federation; 1 Ostrovityanova str., Moscow, 117997, Russia; irvilbulgak@mail.ru
Liliya R. Selimzyanova, MD, Head of the Department of Standardization and Study of the Fundamentals of Evidence-based Medicine at the Scientific Research Institute of Pediatrics and Child Research Institute, Scientific and Clinical Center No. 2 of the Federal State Budgetary Scientific Institution Petrovsky National Research Centre of Surgery, 10 b. 1 Fotieva str., Moscow, 119333, Russia; Associate Professor of the Department of Faculty Pediatrics of the Pediatric Faculty at the Federal State Autonomous Educational Institution of Higher Education N. I. Pirogov Russian National Research Medical University of the Ministry of Health of the Russian Federation; 1 Ostrovityanova str., Moscow, 117997, Russia; Assistant of the Department of Pediatrics at the Academy of Postgraduate Education of the Federal State Budgetary Institution Federal Scientific and Clinical Center of the Federal Medical and Biological Agency of Russia; 91 Volokolamskoe shosse, Moscow, 125310, Russia; lilysir@mail.ru
Tatyana E. Privalova, MD, Associate Professor of the Department of Faculty Pediatrics of the Pediatric Faculty at the Federal State Autonomous Educational Institution of Higher Education N. I. Pirogov Russian National Research Medical University of the Ministry of Health of the Russian Federation; 1 Ostrovityanova str., Moscow, 117997, Russia; Leading Researcher of the Department of Development of Scientific approaches to immunization of patients with Health Disorders and Chronic Diseases at the Scientific Research Institute of Pediatrics and Child Research Institute, Scientific and Clinical Center No. 2 of the Federal State Budgetary Scientific Institution Petrovsky National Research Centre of Surgery, 10 b. 1 Fotieva str., Moscow, 119333, Russia; privalova-tatyana@yandex.ru
Dilyara A. Yusupova, employee of the «International Biotechnological Center «Generium» Joint Stock Company; building 273 Zavodskaya str., Volginsky settlement, Petushinsky district, Vladimir region, 601125, Russia; dilyara.yus1997@mail.ru
Вакцинопрофилактика гриппа у детей раннего возраста – обзор фактических данных/ В. А. Булгакова, Л. Р. Селимзянова, Т. Е. Привалова, Д. А. Юсупова
Для цитирования: Булгакова В. А., Селимзянова Л. Р., Привалова Т. Е., Юсупова Д. А. Вакцинопрофилактика гриппа у детей раннего возраста – обзор фактических данных // Лечащий Врач. 2022; 10 (25): 55-61. DOI: 10.51793/OS.2022.25.10.009
Теги: инфекция, вирус гриппа, иммунитет, вакцинопрофилактика, детский возраст
Грипп: Патогенез
Статьи
Опубликовано в:
«ГРИПП
Пособие для врачей, Санкт-Петербург — Харьков, 2007»
Входными воротами для вирусов гриппа является эпителий дыхательных путей. Однако организм человека в течение столетий совершенствовал механизмы защиты и первой их линией являются неспецифические факторы. К ним относятся вязкие свойства слизи, постоянное движение ресничек цилиндрического эпителия, неспецифические ингибиторы репликации вируса, которые содержатся в секрете дыхательных путей, макрофаги, захватывающие вирус, секреторный IgA. Факторами защиты являются также лектины С-типа (конагглютинин, манозосвязывающий белок, белки А и D сурфактанта), которые связываются с углеводами вируса, вызывают его агрегацию, приводя к опсонизирующему действию. Для того чтобы произошло инфицирование, вирус должен побороть факторы неспецифической резистентности дыхательных путей. Главной мишенью вируса являются клетки цилиндрического реснитчатого эпителия.
Переборов сопротивление ослабленных ресничек, возбудитель попадает в носоглотку и поддается действию высокоактивного секрета клеток. Белки секрета слизистых желез способны неспецифически ингибировать гемагглютинирующую и инфекционную активность вируса гриппа. Это действие обусловлено наличием в секрете гликопротеидов, которые содержат значительное количество N-ацетилнейраминовой кислоты. Существуют сезонные колебания содержания ингибиторов. Наиболее активны они в летне-осенний период, а в период эпидемии гриппа (зима) содержание ингибиторов снижается. Погибшие клетки отрываются и захватываются макрофагами, а также удаляются с секретом дыхательных путей. В подслизистом слое в результате высвобождения биологически активных веществ (гистамин, серотонин, кинины, простагландины) возникает реакция сосудов, форменных элементов крови, образование мелких тромбов и кровоизлияний, диапедез мо-нонуклеаров и нейтрофильных лейкоцитов, отек, местные нарушения метаболизма, изменения рН среды в кислую сторону и тому подобное. При этом патологический воспалительный процесс наиболее выражен в трахее и бронхах.
Наличие токсикоза при гриппе является существенной особенностью патогенеза. Симптомы интоксикации являются следствием резорбции токсичных субстанций вирусов, продуктов нарушенного обмена веществ, что прямо или опосредованно влияет на органы и системы. Вирус обладает токсическим действием на сосудистую систему, значительно повышая проницаемость и ломкость сосудов, что в комплексе с расстройствами микроциркуляции может приводить к развитию геморрагического синдрома. В возникновении циркуляторных расстройств, кроме прямого действия на сосудистую стенку, большое значение имеет нейротропность вируса. Характерны фазовые повреждения вегетативной нервной системы, касающиеся двух ее частей (симпатической и парасимпатической): гипертензия изменяется гипотензией, тахикардия — брадикардией, повышается секреция слизи в дыхательных путях, появляется потливость.
Проникая в более глубокие слои эпителия, вирус встречается со второй линией специфической обороны (интерферон, циркулирующие антитела классов IgM, IgG, IgE, температурная реакция). Механизмы иммунного ответа при гриппе представлены на рис. 3.
Рис. 3. Механизмы иммунного ответа при гриппе
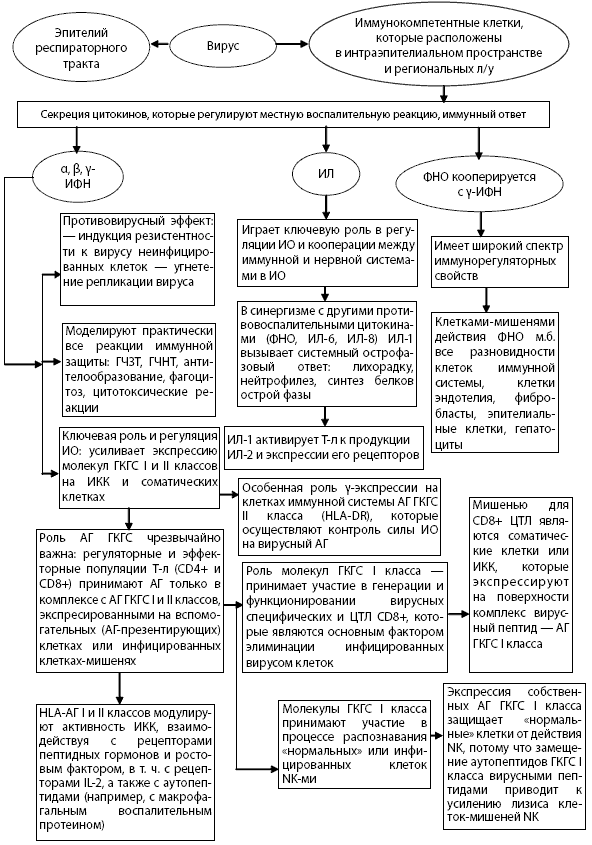
При гриппе в ответ на инфицирование развиваются ранние цитокиновые реакции (РЦР) как наиболее быстрый ответ на вирус. Здесь мы имеем дело с естественным (врожденным) и наиболее распространенным вариантом РЦР на вирус гриппа как на внутриклеточного паразита, когда вирус сам включает систему интерферона, играя роль природного индуктора.
Каскад внутриклеточных событий, который наблюдается после внедрения вируса, обусловлен индукцией образования ИФН и в последующем разрушением вирусных информационных РНК, благодаря действию 2′-5′-олигоаденилсинтетазы и активации эндонуклеазы. Параллельно активированная протеинкиназа фосфорилирует а-субъединицу фактора, который инициирует трансляцию, что приводит к блокировке синтеза вирусных белков. Все это приводит к угнетению репродукции широкого спектра РНК и ДНК-содержащих вирусов за счет прямого внутриклеточного антивирусного эффекта. Эти явления происходят в течение первых часов после проникновения вируса гриппа в организм.
Интерфероны (в первую очередь ИФН-b или так называемые интерфероны I типа) имеют способность к активации естественных киллеров (ЕК) и цитотоксических лимфоцитов. В результате на этом этапе вирусного инфицирования локально осуществляются три взаимосвязанных действия:
- внутриклеточная ингибиция интерферонами репродукции вирусов;
- удаление посредством ЕК и ЦТЛ инфицированного материала;
- защита вновь образованным интерфероном окружающих незараженных клеток от возможного заражения.
Интерферон распределяется по организму, связывается со специфическими рецепторами здоровых неповрежденных клеток и делает их невосприимчивыми к вирусу. С интерферонсвязанных неинфицированных клеток вокруг очага вирусной инфекции образуется заслон для последующего распространения инфекции. Кроме того, интерферон активирует почти все иммунные реакции (модуляция взаимосвязи между эндокринной и иммунной системами, активация макрофагов, повышение цитотоксичности, стимуляция экспрессии антигенов ГКГ I и II классов).
Однако описанные эффекты ИФН нередко являются недостаточными для завершения инфекционного процесса. Подобное имеет место при сниженном сопротивлении организма, дефектности системы ИФН и иммунитета, неблагоприятной экологической ситуации, действии стрессов и др.
В итоге развивается острое заболевание, которое сопровождается продукцией каскада ранних цитокинов (второй этап РЦР), активацией CD4+ и CD8+ Е-клеток с последующим развитием специфического, опосредствованного Т- и В-клеточного иммунитета. В этих случаях кроме ИФН 1-го типа синтезируются такие ранние цитокины, как фактор некроза опухоли, образуются интерлейкины (IL) 1b, 6, 10 и 15, а также трансформирующий фактор роста (TGF). На этом этапе уже отмечается вариабельность РЦР при разных вирусных инфекциях. Продукция ИФН-b считается ключевым доминантным признаком инфицирования вирусом.
ИФН а/b вызывает лейкопению, лимфаденопатию, миграцию клеток из красной пульпы селезенки в белую пульпу, то есть происходит перераспределение клеток для последующих иммунорегуляторных эффектов. ИФН а/b могут усилить специфический иммунный ответ при гриппе в период первичной инфекции за счет притягивания популяции В- и Е-клеток в места воспаления для антигенной презентации.
Первыми на инфекцию начинают реагировать макрофаги, в них происходит расщепление вирусной частицы на отдельные пептиды, которые продвигаются к поверхности клетки, здесь (на мембране макрофага) они контактируют с молекулами ГКГ I и II классов. ИФН, который секретируется ИЛ-1, усиливает экспрессию антигена ГКГ. Выраженное синергичное действие ИЛ-1 и ИЛ-2 способствует пролиферации предшественников Т-клеток в вилочковой железе. В очаг инфекции направляются Т-лимфоциты (хелперы), которым и предоставляются фрагменты антигена в комплексе с молекулами ГКГ. В активации Т-хелперов принимают участие ИЛ-4, ИЛ-6 и ФНО. Возможна ситуация, когда Т-лимфоциты способны непосредственно связывать вирусные антигены при участии антигенов II класса ГКГ. Потом подключаются ЦТЛ и NK-клетки, которые являются основными факторами ликвидации инфицированных вирусом клеток. Но роль CD8+ ЦТЛ двойственна: с одной стороны, они более эффективно по сравнению с другими субпопуляциями элиминируют вирус из отделов нижних дыхательных путей, с другой — усиливают реакции локального воспаления, вызывая в эксперименте синдром респираторного дистресс-синдрома. Результатом этого взаимодействия может стать победа вируса, тогда макроорганизм подключает факторы гуморального иммунитета (местного и общего).
Основу специфического местного иммунитета составляет секреторный IgA. В его синтезе принимают участие клетки реснитчатого эпителия, макрофаги, Т-лимфоциты, клетки секреторного эпителия. Макрофаги, локализованные в пространствах между эпителиальными клетками, захватывают обломки разрушенных вирусом клеток, метаболизируют их. Антигены, подготовленные макрофагами, активизируют Т- и В-лимфоциты, которые превращаются в плазмоциты, продуцируют антитела класса IgA. Выполняя важные эффекторные функции, IgA играет роль молекулы, которая регулирует функции клеток иммунной системы, в частности альвеолярных макрофагов, несущих рецепторы к Fc-фрагменту этого Ig. Так, иммунные комплексы, которые содержат антитела класса А, индуцируют в моноцитах-макрофагах синтез ФНО-а и СЗ-комплемента С. Секреторные IgA связывают вирус и препятствуют его выходу из организма в активной форме, что ограничивает циркуляцию вируса среди людей.
При первой встрече с вирусом через 3-5 дней образуются антитела класса IgM. Повышение их содержания свидетельствует об остроте инфекционного процесса. Высокое содержание Ig в крови является показателем устойчивости организма к инфекции. IgE — единственный тип антител, который вступает во взаимодействие с мембраной тучных клеток (в клинической картине наблюдаются приступы бронхоспазма).
Иммунные механизмы при первичной встрече с вирусом запоминаются организмом в виде информации, заложенной в клетки памяти (иммунологическая память), и при повторной встрече с вирусом той же антигенной разновидности иммунные реакции протекают быстрее и более эффективно. Создание иммунной памяти об антигене является целью применения вакцин. С их помощью создается и поддерживается защитная концентрация противогриппозных антител. Антитела, вступая во взаимосвязь с антигеном, образуют иммунные комплексы. Иногда вместе с защитными функциями они могут стать причиной тяжелых иммунопатологических состояний. Циркулируя по всему организму, они оседают в тканях, вызывая воспалительные реакции в капиллярах клубочков почек и синовиальных оболочек суставов. Частично вирус из организма выделяется почками, что, возможно, и обусловливает тот факт, что в эпителии дистальных канальцев, как и в эндотелии капилляров клубочков, оказывается значительное количество антигена вируса. Почками также выделяются иммунные комплексы, фрагменты клеток, что приводит к сенсибилизации тканей почки и впоследствии, через несколько недель и даже месяцев после перенесенного заболевания, может послужить причиной возникновения гломерулонефрита. Инициатором в этом случае может быть фактор, который имеет антигенную природу (например, переохлаждение).
Находясь в окружении антител, вирус может сохранять свою структуру и при разрушении комплекса опять поражать чувствительные клетки. Длительная циркуляция комплексов приводит к инфицированию все большего количества клеток, к поддержке инфекции и к персистенции. В данное время не исключается возможность длительной персистенции вируса гриппа в ЦНС по типу медленной инфекции с развитием впоследствии такого патологического состояния, как паркинсонизм. Это изменяет представление о гриппе как об острой инфекции. Установлено, что в 50% случаев антиген вируса гриппа сохраняется в периферических лимфоидных клетках и в крови до 120-200 и более дней.
При гриппе роль антигена могут играть не только структура вируса, но и измененные вирусом структуры клеток, и уже к ним синтезируются антитела, с которыми начинают вступать во взаимодействие нормальные клетки, в результате чего возникает угроза развития аутоиммунопатологического состояния.
Изменения во внутренних органах однотипны, обусловлены генерализованной вазодилятациеи. При массивной вирусемии, которая быстро развивается в первые часы болезни, может возникнуть инфекционно-токсический шок с развитием сердечно-сосудистой недостаточности. В его основе лежат несколько факторов: сосудистый (непосредственное действие вируса на сосуды с повышением их проницаемости, вазодилятациеи), геморрагический синдром с повреждением надпочечников и дефицитом гормонов, нарушение функции миокарда. У таких больных смерть может наступить в ближайшие часы от начала заболевания.
В результате токсического повреждения сосудистого аппарата ЦНС наступает гиперсекреция спинномозговой жидкости, нарушается ликвородинамика, что приводит к повышению внутричерепного давления, может наступить отек мозга. Чаще все-таки повреждаются мягкие мозговые оболочки, сосудистое сплетение, где можно выявить антигены вируса гриппа.
Инфекционно-алергический процесс после перенесенной гриппозной инфекции может возникнуть также в эндокарде. Изменения в миокарде, определенные на ЭКГ как миокардиодистрофия, обусловлены токсикозом и циркуляторными расстройствами.
В патогенезе отека легких имеют значение много факторов: нарушения гемодинамики, связанные с токсикозом, воспалительные процессы в бронхах и легких, снижение сократительной функции левого желудочка, что чаще развивается у лиц с сопутствующими заболеваниями сердечно-сосудистой системы. Необходимо подчеркнуть, что начальные стадии отека легких, на которых повреждается интерстициальная ткань, определяются лишь рентгенологически в виде нерезких, расплывчатых теней, которые сливаются и распространяются от корней к периферии легочных полей.
В механизмах устойчивости организма к генетически инородной информации принимают участие два основных феномена: наследственная резистентность и приобретенный иммунитет:
- природная видовая наследственная резистентность, связанная с врожденной стойкостью организма, которая развивается с возрастом, к возбудителям инфекций, основанная на отсутствии чувствительных клеток или повышении их резистентности к репродукции вируса, а также на их биологической инактивации при участии интерферона, фагоцитарных факторов, нормальной температуры тела или неспецифических ингибиторов крови;
- приобретенный иммунитет создается после болезни или искусственной иммунизации вакцинами.
Приобретенный иммунитет опирается на формирование местной секреторной защиты. Секреторный иммунитет предупреждает или смягчает тяжесть заболевания во входных воротах гриппозной инфекции при участии антител класса IgA, которые синтезированы в процессе кооперации между В-лимфоцитами и эпителиальными клетками. Секреторные антитела избирательно адсорбируются на поверхности клеток мерцательного эпителия, эффективно защищая их от инвазии вируса.
Длительность противогриппозного иммунитета ограничена не дву-мя-тремя годами, как это считалось бесспорным до 1977 г. (в этот год особенно тяжело болели молодые люди, рожденные после 1957 г., когда вирус A (H1N1) исчез из циркуляции и появился снова в 1977 г.). В случае возвращения к активной циркуляции уже известного подтипа через 20 и более лет — выявляется сохранение специфической невосприимчивости к возбудителю, который вернулся, у части населения, которая контактировала с ним раньше. Такая длительная иммунологическая память обусловлена, конечно, не антителами (их титры в крови падают ниже защитного порога через 6-12 месяцев, а в секрете дыхательных путей — еще быстрее). Длительный постинфекционный иммунитет обеспечивают клеточные механизмы (Т- и В-лимфоциты), в том числе местные, во входных воротах возбудителя инфекции. Существует четко выраженная корреляция невосприимчивости к гриппу с концентрацией антител в крови (в основном IgG) и в секрете дыхательных путей (IgA). Однако в частных случаях гриппом могут заболеть люди с высоким исходным уровнем гуморального иммунитета и не заболевают инфицированные лица с низким начальным титром антител. Такие примеры подчеркивают сложность и многогранность иммунной защиты организма, где роль отдельных факторов интегрирована в общем результате.
Между специфическими механизмами противогриппозного иммунитета существует распределение защитных функций:
- секреторные антитела, которые подавляют репродукцию вируса во входных воротах инфекции, обеспечивают противоэпидемическую защиту, направленную на ограничение рассеивания и передачи возбудителя от инфицированных лиц здоровому окружению; в связи с широким диапазоном нейтрализующего эффекта секреторные антитела способны подавлять любые антигенные варианты вируса гриппа А в пределах своего подтипа;
- сывороточные антитела нейтрализуют токсичные продукты вируса и регулируют клиническую тяжесть болезни;
- клеточно-обусловленные факторы иммунитета устраняют резервуар вируса в инфицированных клетках, малодоступных влиянию антител.
Напряженность противовирусного иммунитета зависит от уровня циркулирующих антител и образования цитотоксических лимфоцитов. Цитотоксические лимфоциты вызывают лизис инфицированных вирусом клеток.
Повторное заболевание гриппом обусловлено высокой изменчивостью вируса гриппа и формированием иммунитета только к конкретному штамму, что и объясняет необходимость ежегодной вакцинации.
«ГРИПП
Пособие для врачей, Санкт-Петербург — Харьков, 2007»
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)




